Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
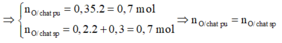
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
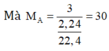
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.

Gọi 3a là số mol CO2 \(\rightarrow\)nH2O=2a mol
BTKL ta có
44.3a+18.2a=18+16,8/22,4.32
\(\rightarrow\)a=0,25 mol
\(\rightarrow\)nCO2=0,75 mol nH2O=0,5 mol
\(\rightarrow\)nC=0,75 mol nH=1 mol
Ta có 0,75.12+1=10<18 \(\rightarrow\) Trong A có O
mO trong A=18-10=8 g
nO=\(\frac{8}{16}\)=0,5 mol
Gọi CTHH là CxHyOz
Ta có x: y: z=nC: nH : nO=0,75 : 1 : 0,5 =3:4:2
\(\rightarrow\)CT đơn giản nhất là C3H4O2
mà MA=36x2=72
\(\rightarrow\)72n=72\(\rightarrow\)n=1
Vậy CTPT của A là C3H4O2

Ta có: \(\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{5}{6}< 1\)
⇒ X là ankan
PTHH: CnH2n+2 + \(\dfrac{3n+1}{2}\)O2 \(\underrightarrow{to}\) nCO2 + \(\left(n+1\right)\)H2O
\(n_{O_2}=\dfrac{35,84}{22,4}=1,6\left(mol\right)\)
Theo PT: \(n_{C_nH_{2n+2}}=\dfrac{2}{3n+1}n_{O_2}=\dfrac{2}{3n+1}\times1,6=\dfrac{3,2}{3n+1}\left(mol\right)\)
\(\Rightarrow M_{C_nH_{2n+2}}=14,4\div\dfrac{3,2}{3n+1}=13,5n+4,5\)
\(\Leftrightarrow12n+2n+2=13,5n+4,5\)
\(\Leftrightarrow0,5n=2,5\)
\(\Leftrightarrow n=5\)
Vậy CTPT của X là C5H12

Biết 1 lít hỗn hợp A ở dạng khí nặng gấp hai lần 1 lít khí C 2 H 6 ở cùng điều kiện.
⇒ n A = n C 2 H 6 ⇒ M A = 2 M C 2 H 6
(cùng điều kiện nên tỉ lệ thể tích chính là tỉ lệ số mol)
Ba chất có cùng công thức phân tử ⇒ có cùng khối lượng mol phân tử : M = 2.30 = 60 (gam/mol). Khi đốt cháy hỗn hợp A thu được CO 2 , H 2 O → công thức phân tử của các chất có dạng C x H y O z
Phương trình hoá học
C x H y O z + (x + y/4 - z/2) O 2 → x CO 2 + y/2 H 2 O
CO 2 + Ca OH 2 → Ca CO 3 + H 2 O
Ta có : n CO 2 = n CaCO 3 = 15/100 = 0,15mol
Theo định luật bảo toàn khối lượng, ta có :
m A + m O = m CO 2 + m H 2 O
⇒ 3 + 7,2 = 0,15 x 44 + m H 2 O ⇒ m H 2 O = 3,6g
n A = 3/60 = 0,05mol; n CO 2 = 0,05x = 0,15 ⇒ x = 3
n H 2 O = 0,05y/2 = 3,6/18 ⇒ y = 8
M A = 12x + y + 16z = 60 ⇒ z = 1 ⇒ ông thức phân tử của A là C 3 H 8 O
Công thức cấu tạo của ba chất là : CH 3 CH 2 CH 2 OH
CH 3 CHOH CH 3
CH 3 -O- CH 2 CH 3

Gọi \(\left\{{}\begin{matrix}n_{CO}=a\left(mol\right)\\n_{C_nH_{2n+2}}=b\left(mol\right)\end{matrix}\right.\)
=> \(a+b=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Bảo toàn C: \(a+bn=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Bảo toàn H: \(2bn+2b=\dfrac{2,7}{18}.2=0,3\left(mol\right)\)
=> a = 0,15; b = 0,05; n = 2
=> CTPT: C2H6
\(\left\{{}\begin{matrix}\%V_{C_2H_6}=\dfrac{0,05}{0,2}.100\%=25\%\\\%V_{CO}=\dfrac{0,15}{0,2}.100\%=75\%\end{matrix}\right.\)

\(n_{C_2H_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: C2H4 + 3O2 ---to---> 2CO2 + 2H2O
0,2 0,6 0,4 0,4
VO2 = 0,6.22,4 = 13,44 (l)
mCO2 = 0,4.44 = 17,6 (g)
mH2O = 0,4.18 = 7,2 (g)
PTHH: Ca(OH)2 + CO2 ---> CaCO3 + H2O
Khối lượng dd tăng bằng khối lượng CO2 tham gia phản ứng là 17,6 g

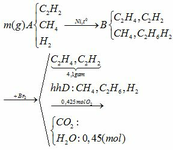
C2H2 + H2 C2H4
C2H2 + H2 C2H6
Khi cho hỗn hợp B qua dd nước Br2 chỉ có C2H4 và C2H2 phản ứng C2H2 +2Br2 → C2H2Br4
C2H4 + Br2 → C2H4Br2
=> khối lượng bình Br2 tăng chính bằng khối lượng của C2H2 và C2H4
mC2H2 + mC2H4 = 4,1 (g)
Hỗn hợp khí D đi ra là CH4, C2H6 và H2
CH4 + 2O2 → t ∘ CO2 + 2H2O
C2H6 + O2 → t ∘ 2CO2 + 3H2O
2H2 + O2 → t ∘ 2H2O
Bảo toàn nguyên tố O cho quá trình đốt cháy hh D ta có:
2nCO2 = 2nO2 – nH2O => nCO2 = ( 0,425. 2– 0,45)/2 = 0,2 (mol)
Bảo toàn khối lượng : mhh D = mCO2 + mH2O – mO2 = 0,2.44 + 0,45.18 – 0,425.32 = 3,3 (g)
Bảo toàn khối lương: mA = (mC2H2 + mC2H4) + mhh D = 4,1 + 3,3 = 7,4 (g)
\(n_{H_2}=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
\(Đăt:n_{CO_2}=3a\left(mol\right),n_{H_2O}=4a\left(mol\right)\)
\(BTKL:\)
\(6+0.45\cdot32=3a\cdot44+4a\cdot18\)
\(\Rightarrow a=0.1\)
\(m_O=6-0.3\cdot12-0.4\cdot2=1.6\left(g\right)\)
\(n_O=\dfrac{1.6}{16}=0.1\left(mol\right)\)
\(CT:C_xH_yO_z\)
\(x:y:z=0.3:0.8:0.1=3:8:1\)
\(CTPT:C_3H_8O\)