Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Khi bọt khí bắt đầu thoát ra ở catot là thời điểm Ag+ và Cu2+ đều bị điện phân hết.
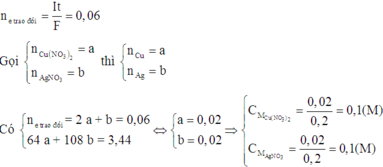

Đáp án A
- Phương trình điện phân
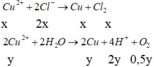
Có mdung dịch giảm = m Cu + m Cl 2 + m O 2 = 64 ( x + y ) + 71 x + 32 . 0 , 5 y = 20 , 815 gam
Cho (Mg, MgO) + dung dịch sau điện phân → 18,16g muối + 0,012mol khí Y
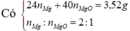
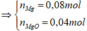
m muối = m Mg ( NO 3 ) 2 + m NH 4 NO 3 = 148 . ( 0 , 08 + 0 , 04 ) + 80 n NH 4 NO 3 = 18 , 16 g ⇒ n NH 4 NO 3 = 0 , 005 mol
+ Giả sử 1 mol N+5 nhận n mol e để chuyển thành N trong khí Y
Áp dụng bảo toàn electron có:
![]()
=> n = 10 => Khí Y là N2
m muối = m Mg ( NO 3 ) 2 + m NH 4 NO 3 = 148 . ( 0 , 08 + 0 , 04 ) + 80 n NH 4 NO 3 = 18 , 16 g ⇒ 2 y = 2 n Mg ( NO 3 ) 2 + 2 n NH 4 NO 3 + 2 n N 2 = 0 , 274 mol
=>Thời gian điện phân t = ( 0 , 137 + 0 , 073 ) . 2 . 96500 5 = 8016 s

Đáp án A
- Khí bắt đầu thoát ra ở catot là khi Fe3+, Cu2+ bị điện phân hết, H+ vừa bị điện phân
Phương trình điện phân:
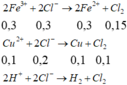
- Thêm dung dịch AgNO3 vừa đủ vào
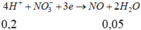
=> m Y =200+250-156,65-30.0,05-71.0,25=274,1 g
- Dung dịch Y Chứa 2 muối là: Fe(NO3)3 ; Cu(NO3)2
Muối có phân tử khối lớn hơn là Fe(NO3)3
C % Fe ( NO 3 ) 3 = 242 . 0 , 3 274 , 1 . 100 % = 26 , 49 % gần với giá trị 27 phút

Giải thích: Đáp án A
Khi điện phân t (s)
43,24 = (M + 96).x + 58,5.y(1)
Catot(-) : M2+ + 2e -> M
Mol x -> 2x
2H2O + 2e -> H2 + 2OH-
Mol (0,4 – 2x)
Anot(+) : 2Cl- -> Cl2 + 2e
ne = 0,4 mol
=> nCl2 = 0,2 mol ; nNaCl = 0,4 mol = y
=> (M + 96)x = 19,84(2)
(Vì điện phân chỉ ngừng khi nước bắt đầu điện phân ở cả 2 điện cực, mà ở Anot chỉ có Cl2
=> nước chưa bị điện phân ở anot)
Với 2t (s) => ne = 0,8 mol
Anot : 2H2O + 2e -> O2 + 4H+ + 4e
=> mdd giảm = M.x + 2.(0,2 – x + 0,2) + 0,2.71 + 0,1.32 = 25,496(3)
Từ (2,3) => x = 0,128 ; M = 59 (Ni)
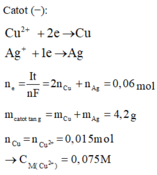







2 giờ = 7200 s
Gọi thời gian điện phân muối bạc là t1
Gọi thời gian điện phân muối đồng là t2
⇒ t1 + t2 = 7200 (1)
Theo định luật Faraday:
mà mAg + mCu = 3,44 (g) ⇒ (9.t1 + 2,666.t2 ). 10-4 = 3,44 (2)
(1),(2) ⇒ t1 = 2400 (s) ⇒ mAg = 2,16 gam ⇒ nAg = 0,02
t2 = 4800 (s) ⇒ mCu = 1,28 gam ⇒ nCu = 0,02
CM Cu(NO3)2 = 0,02/0,2 = 0,1M ; CM AgNO3 = 0,02/0,2 = 0,1 M