Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Theo định luật Faraday: m = AIt/nF => I = mnF/At : 80% = 3,75 (A)

Đáp án B
Theo định luật II của Pha – ra – đây thì khối lượng Ag sinh ra ở catot là:
m = 1 F . A n . It = 1 96500 . 108 1 . 5 . 15 . 60 = 5 , 036 ( g )

Đáp án B
Phản ứng điện phân:
4 AgNO 3 + 2 H 2 O → đpdd 4 Ag + O 2 + 4 HNO 3 a a 0 , 25 a a
Theo đề bài, sau điện phân thì ngắt dòng điện, sau khi các phản ứng xảy ra hoàn toàn thì thu được hỗn hợp khí X gồm NO2 => 2 khả năng:
Phản ứng hòa tan Ag bởi HNO3 tạo ra NO2.
Phản ứng hòa tan Ag tạo ra NO, sau đó NO + O 2 → NO 2 (thu được hỗn hợp NO2 và O2 dư)
Do đề yêu cầu m lớn nhất nên sản phẩm khử phải nhận nhiều e nhất => đó là NO
3 Ag + 4 HNO 3 → 3 AgNO 3 + NO + 2 H 2 O ban đầu : a a mol phản ứng 3 4 a a a 4 mol 2 NO + O 2 → 2 NO 2 ban đầu a 4 a 8 mol phản ứng a 4 a 8 a 4 mol
Vậy khi đó sau phản ứng sẽ có:
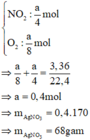

Đáp án A
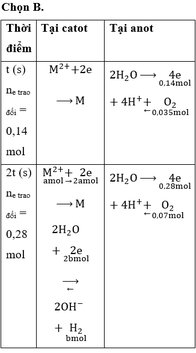
- 2 bình mắc nối tiếp nên dòng điện chạy qua có cùng cường độ
Đổi 3 phút 13 giây = 193 giây; 9 phút 39 giây = 579 giây
- Phương trình điện phân
Bình 1:
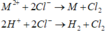
Bình 2: ![]()
+ Bình 2:
![]()
=> Chứng tỏ Ag+ còn dư sau khi điện phân 193s, có thể còn dư sau điện phân 579s
Điện phân 193s :
![]()
+ Bình 1:
![]()
=> Chứng tỏ M2+ ở bình 1 bị điện phân trước, sau khi điện phân 193s thì M2+ còn dư; sau khi điện phân 579s thì M2+ hết; H+ đã bị điện phân
Điện phân 193s:
![]()
=> M là Cu => 0,8 a = 3 , 2 64 => a = 0,0625(M)
![]()