
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

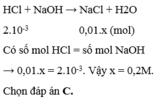

Đáp án C
nHCl = 0,1.0,02=0,002 (mol)
NaOH + HCl →NaCl + H2O
0,002←0,002 (mol)
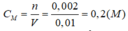

Đáp án A
Số mol HCl là: n HCl = 0 , 01 . 0 , 1 = 0 , 001 mol
Phương trình hóa học: HCl + NaOH → NaCl + H 2 O
Phản ứng trung hòa là phản ứng xảy ra vừa đủ giữa axit và bazơ để tạo muối trung hòa:


Các PTHH:
Fe + S → FeS (1)
FeS + 2HCl → Fe Cl 2 + H 2 S (2)
Fe(dư) + 2HCl → Fe Cl 2 + H 2 (3)
HCl (dư) + NaOH → NaCl + H 2 O (4)
Nồng độ mol của dung dịch HCL :
Tổng số mol HCL tham gia các phản ứng (2), (3), (4) :
0,1 + 0,1 + 0,0125 = 0,2125 (mol)
Nồng độ mol của dung dịch HCl : 0,2125/0,5 = 0,425 (mol/l)

HCl+NaOH => NaCl+\(H_2O\)
\(n_{NaOH}=C_M.V=0,3.0,2=0,06\) (mol)
=> \(n_{HCl}=n_{NaOH}=0,06\) (mol)
=> \(V_{HCl}=\dfrac{n}{C_M}=\dfrac{0,06}{0,4}=0,15\)(l)=150(ml)
=> C

Câu 2 :
$n_{HCl} = 0,2.1 + 0,3.1,5 = 0,65(mol)$
$V_{dd} = 0,2 + 0,3 = 0,5(mol)$
$C_{M_{HCl}} = \dfrac{0,65}{0,5} =1,3M$
Câu 3 :
Gọi $m_{H_2O\ cần\ thêm} =a (gam)$
Sau khi thêm :
$m_{NaOH} = 100.35\% = 35(gam)$
$m_{dd} = 100 + a(gam)$
Suy ra: $\dfrac{35}{100 + a}.100\% = 20\%$
Suy ra: a = 75(gam)
Câu 4 :
Gọi $V_{dd\ HCl\ 2M} =a (lít) ; V_{dd\ HCl\ 3M} = b(lít)$
Ta có :
$a + b = 4$
$2a + 3b = 4.2,75$
Suy ra a = 1(lít) ; b = 3(lít)

\(a,n_{H_2SO_4}=1.0,1=0,1(mol)\\ PTHH:2NaOH+H_2SO_4\to Na_2SO_4+2H_2O\\ \Rightarrow n_{naOH}=2n_{H_2SO_4}=0,2(mol)\\ \Rightarrow m_{dd_{NaOH}}=\dfrac{0,2.40}{10\%}=80(g)\\ b,m_{dd_{H_2SO_4}}=1,2.100=120(g)\\ n_{Na_2SO_4}=0,1(mol)\\ \Rightarrow C\%_{Na_2SO_4}=\dfrac{0,1.142}{80+120}.100\%=7,1\%\)

Ta có:
\(n_{HCl\left(D\right)}=n_{NaOH}=\frac{0,1.15}{1000}=0,0015\left(mol\right)\)
\(PTHH:NaOH+HCl\rightarrow NaCl+H_2O\)
\(AgNO_3+HCl\rightarrow AgCl+HNO_3\)
\(\Rightarrow CM_D=\frac{0,0015}{0,01}=0,15M\)
\(n_{HCl\left(E\right)}=n_{AgCl}=\frac{2,87}{143,5}=0,02\left(mol\right)\)
\(\Rightarrow CM_E=\frac{0,02}{0,08}=0,25M\)
Giải hệ PT:
\(\left\{{}\begin{matrix}3a+b=10\\a+3b=0,6\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,3\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}CM_A=0,3M\\CM_B=0,1M\end{matrix}\right.\)

\(C_{M_{ddNaOH}}=\dfrac{0,1}{0,5}=0,2M\)
mdd = 0,2.40 + 1.500 = 508 (g)
\(C\%_{ddNaOH}=\dfrac{0,2.40.100\%}{508}=1,57\%\)