Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Gọi số mol Zn, Fe là a, b (mol)
=> 65a + 56b = 8,56 (1)
\(n_{H_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
a--->2a-------->a----->a
Fe + 2HCl --> FeCl2 + H2
b----->2b------->b------>b
=> a + b = 0,14 (2)
(1)(2) => a = 0,08; b = 0,06
=> \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,08.65}{8,56}.100\%=60,748\%\\\%m_{Fe}=\dfrac{0,06.56}{8,56}.100\%=39,252\%\end{matrix}\right.\)
b)
nKOH = 0,2.0,1 = 0,02 (mol)
PTHH: KOH + HCl --> KCl + H2O
0,02-->0,02
=> nHCl = 0,02 + 2a + 2b = 0,3 (mol)
=> \(C_{M\left(HCl\right)}=xM=\dfrac{0,3}{0,15}=2M\)
c) m = 0,08.136 + 0,06.127 = 18,5(g)

a) Gọi số mol Zn, Fe là a, b (mol)
=> 65a + 56b = 7,35 (1)
PTHH: Zn + 2HCl --> ZnCl2 + H2
a---->2a------->a------>a
Fe + 2HCl --> FeCl2 + H2
b------>2b----->b------>b
=> \(a+b=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
=> a + b = 0,12 (2)
(1)(2) => a = 0,07; b = 0,05
=> \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,07.65}{7,35}.100\%=61,9\%\\\%m_{Fe}=\dfrac{0,05.56}{7,35}.100\%=38,1\%\end{matrix}\right.\)
b) nHCl(dư) = 0,3.1 - 0,07.2 - 0,05.2 = 0,06 (mol)
PTHH: Ca(OH)2 + 2HCl --> CaCl2 + 2H2O
0,03<-----0,06
=> \(x=C_{M\left(ddCa\left(OH\right)_2\right)}=\dfrac{0,03}{0,1}=0,3M\)
c) Chất rắn thu được là Fe2O3
Bảo toàn Fe: \(n_{Fe_2O_3}=0,025\left(mol\right)\)
=> \(a=m_{Fe_2O_3}=0,025.160=4\left(g\right)\)
Kết tủa thu được là Fe(OH)2
Bảo toàn Fe: \(n_{Fe\left(OH\right)_2}=0,05\left(mol\right)\)
=> \(m=m_{Fe\left(OH\right)_2}=0,05.90=4,5\left(g\right)\)

a) Gọi số mol Mg, Fe là a, b (mol)
=> 24a + 56b = 11,84
\(n_{HCl}=\dfrac{146.14\%}{36,5}=0,56\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
a--->2a--------->a----->a
Fe + 2HCl --> FeCl2 + H2
b-->2b-------->b------>b
=> 2a + 2b = 0,56
=> a = 0,12; b = 0,16
=> \(\left\{{}\begin{matrix}\%Mg=\dfrac{0,12.24}{11,84}.100\%=24,324\%\\\%Fe=\dfrac{0,16.56}{11,84}.100\%=75,676\%\end{matrix}\right.\)
b) \(n_{H_2}=a+b=0,28\left(mol\right)\)
=> \(V_{H_2}=0,28.22,4=6,272\left(l\right)\)
c) mdd sau pư = 11,84 + 146 - 0,28.2 = 157,28 (g)
=> \(\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,12.95}{157,28}.100\%=7,25\%\\C\%_{FeCl_2}=\dfrac{0,16.127}{157,28}.100\%=12,92\%\end{matrix}\right.\)

a, Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 56y = 13,8 (1)
BTNT Al và Fe, có: \(\left\{{}\begin{matrix}n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{2}x\left(mol\right)\\n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=\dfrac{1}{3}y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\dfrac{1}{2}x.102+\dfrac{1}{3}y.232=21,8\left(g\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{13,8}.100\%\approx39,1\%\\\%m_{Fe}\approx60,9\%\end{matrix}\right.\)
b, BTNT O, có: \(n_{O_2}=\dfrac{3n_{Al_2O_3}+4n_{Fe_3O_4}}{2}=0,6\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,6.22,4=13,44\left(l\right)\)
Bạn tham khảo nhé!

Mg+2HCl->MgCl2+H2
x------------------------x
Zn+2HCl->ZnCl2+H2
y-----------------------y
=>Ta có :\(\left\{{}\begin{matrix}24x+65y=15,4\\x+y=0,3\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}x=0,1mol\\y=0,2mol\end{matrix}\right.\)
=>m Mg=0,1.24=2,4g
=>m Zn=0,2.65=13g
b)VHCl=\(\dfrac{0,1.2+0,2.2}{2}\)=0,3l=300ml

ta có :
2Mg+O2-to>2MgO
x--------0,5x
2Zn+O2-to>2ZnO
y-------0,5y
=>\(\left\{{}\begin{matrix}24x+65y=14,58\\0,5x+0,5y=0,15\end{matrix}\right.\)
=>x=0,12 mol ,y=0,18 mol
=>%mMg=\(\dfrac{0,12.24}{14,58}100\)=19,753%
=>%mZn=80,247%
\(n_{O_2}=\dfrac{4,8}{32}=0,15mol\)
Gọi \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Zn}=y\end{matrix}\right.\)
\(2Mg+O_2\rightarrow\left(t^o\right)2MgO\)
x 1/2 x ( mol )
\(2Zn+O_2\rightarrow\left(t^o\right)2ZnO\)
y 1/2 y ( mol )
Ta có:
\(\left\{{}\begin{matrix}24x+65y=14,58\\\dfrac{1}{2}x+\dfrac{1}{2}y=0,15\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,12\\y=0,18\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Mg}=0,12.24=2,88g\\m_{Zn}=0,18.65=11,7g\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{2,88}{14,58}.100=19,75\%\\\%m_{Zn}=100\%-19,75\%=80,25\%\end{matrix}\right.\)

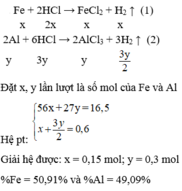
Gọi nZn = a (mol); nFe = b (mol)
=> 65a + 56b = 29,8 (1)
VO2 = 6,72/22,4 = 0,3 (mol)
PTHH:
2Zn + O2 -> (t°) 2ZnO
a ---> 0,5a ---> a
3Fe + 2O2 -> (t°) Fe3O4
b ---> 2b/3 ---> b/3
=> 0,5a + 2b/3 = 0,3 (2)
Từ (1)(2) => a = 0,2 (mol); b = 0,3 (mol)
=> mZn = 0,2 . 65 = 13 (g)
=> mFe = 0,3 . 56 = 16,8 (g)
PTHH:
Zn + 2HCl -> ZnCl2 + H2
0,2 ---> 0,4
Fe + 2HCl -> FeCl2 + H2
0,3 ---> 0,6
=> mHCl = (0,6 + 0,4) . 36,5 = 36,5 (g)
=> mddHCl = 36,5/3,65% = 1000 (g)
Số mol khí oxi cần dùng là 6,72/22,4=0,3 (mol).
BTKL: 65nZn+56nFe=29,8 (1).
BTe: 2nZn+(8/3)nFe=2nO \(\Leftrightarrow\) 6nZn+8nFe=3,6 (2).
Giải hệ phương trình gồm (1) và (2), ta suy ra nZn=0,2 (mol) và nFe=0,3 (mol).
Phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu:
%mZn=0,2.65/29,8\(\approx\)43,62% \(\Rightarrow\) %mFe\(\approx\)100%-43,62%\(\approx\)56,38%.
Số mol HCl cần dùng để hòa tan hồn hợp ban đầu là:
nHCl=2nZn+2nFe=2.0,2+2.0,3=1 (mol).
Khối lượng dung dịch HCl cần dùng là:
m=1.36,5/3,65%=1000 (g).