Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

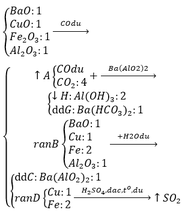
Chọn A
Dung dịch nước vôi trong là Ca ( O H ) 2 là dung dịch bazơ
=> Oxit axit có thể tác dụng với dung dịch bazơ, đó là C O 2 và S O 2 và 2 khí này bị hấp thụ trong dd
CO không tác dụng vì CO là oxit trung tính.
=> Khí thoát ra là CO

\(V_{C_2H_6}=13,44-6,72=6,72\left(l\right)\)
=> \(n_{C_2H_6}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{C_2Ag_2}=\dfrac{24}{240}=0,1\left(mol\right)\)
=> \(n_{C_2H_2}=0,1\left(mol\right)\)
=> \(n_{C_2H_4}=\dfrac{13,44}{22,4}-0,3-0,1=0,2\left(mol\right)\)
=> \(\left\{{}\begin{matrix}\%m_{C_2H_6}=\dfrac{0,3.30}{0,3.30+0,2.28+0,1.26}.100\%=52,326\%\\\%m_{C_2H_4}=\dfrac{0,2.28}{0,3.30+0,2.28+0,1.26}.100\%=32,558\%\\\%m_{C_2H_2}=\dfrac{0,1.26}{0,3.30+0,2.28+0,1.26}.100\%=15,116\%\end{matrix}\right.\)

CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,34 ←0,34
CO + O(Oxit) → CO2
Nhận thấy:
nO = nCO2
mX = mO (oxit) + mY
=> mY = 37,68 – 16 . 0,34 = 32,24g

\(n_{\downarrow}=\dfrac{35}{100}=0,35mol\Rightarrow n_C=m_{CaCO_3}=0,35mol\)
\(\left\{{}\begin{matrix}CH_4:x\left(mol\right)\\C_2H_2:y\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x+y=\dfrac{4,48}{22,4}=0,2\\BTC:x+2y=0,35\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,15\end{matrix}\right.\)
\(m_{tăng}=m_{Br_2}=2n_{C_2H_2}\cdot160=48g\)
\(\%V_{CH_4}=\dfrac{0,05}{0,05+0,15}\cdot100\%=25\%\)
\(\%V_{C_2H_2}=100\%-25\%=75\%\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_2}=y\end{matrix}\right.\)
\(n_{hh}=\dfrac{4,48}{22,4}=0,2mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(2C_2H_2+5O_2\rightarrow\left(t^o\right)4CO_2+2H_2O\)
y 2y ( mol )
\(n_{CaCO_3}=\dfrac{35}{100}=0,35mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,35 0,35 ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,2\\x+2y=0,35\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,15\end{matrix}\right.\)
\(m_{tăng}=2m_{C_2H_2}=2.0,15.160=48g\)
\(V_{CH_4}=0,05.22,4=1,12l\)
\(V_{C_2H_2}=0,15.22,4=3,36l\)

a)
CH4 + 2O2 --to--> CO2 + 2H2O
C2H4 + 3O2 --to--> 2CO2 + 2H2O
b) Gọi số mol CH4, C2H4 là a, b (mol)
=> \(a+b=\dfrac{6,72}{22,4}=0,3\)
\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
Khí thoát ra khỏi bình là CH4
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
a---------------->a
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,2<------0,2
=> a = 0,2 (mol)
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,2}{0,3}.100\%=66,67\%\\\%V_{C_2H_4}=100\%-66,67\%=33,33\%\end{matrix}\right.\)
c) b = 0,1 (mol)
CH4 + 2O2 --to--> CO2 + 2H2O
0,2--------------->0,2----->0,4
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,1----------------->0,2---->0,2
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,4------>0,4
=> \(m_{CaCO_3}=0,4.100=40\left(g\right)\)
\(\left\{{}\begin{matrix}m_{CO_2}=44\left(0,2+0,2\right)=17,6\left(g\right)\\m_{H_2O}=\left(0,4+0,2\right).18=10,8\left(g\right)\end{matrix}\right.\)
Xét \(\Delta m=m_{CO_2}+m_{H_2O}-m_{CaCO_3}=17,6+10,8-40=-11,6\left(g\right)\)
=> Khối lượng dd giảm 11,6 gam

\(n_{hhk}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
`->` Khí thoát ra là CH4
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,2 0,2 ( mol )
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,2 0,2 ( mol )
\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
\(\%V_{CH_4}=\dfrac{0,2}{0,3}.100=66,67\%\)
\(\%V_{C_2H_4}=100-66,67=33,33\%\)
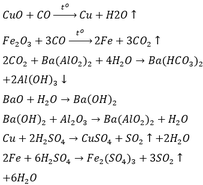
Đáp án
A.Dẫn hỗn hợp qua dung dịch Ca(OH)2 dư.
CO2 + Ca(OH)2 ---> CaCO3 + H2O
Có thể tinh chế CO ra khỏi hỗn hợp ( CO + CO2 ) bằng cách :
A. Dẫn hỗn hợp qua dung dịch Ca(OH)2 dư
B. Dẫn hỗn hợp qua dung dịch PbCl2 dư
C. Dẫn hỗn hợp qua NH3
D. Dẫn hỗn hợp qua dung dịch Cu(NO3)2 dư
Trả lời:
A. Dẫn hỗn hợp qua dung dịch Ca(OH)2 dư
PTHH: CO2 + Ca(OH)2 ------> CaCO3 + H2O