Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Tốc độ phản ứng tỷ lệ thuận với nồng độ của chất phản ứng: v = k A a * B b

a) 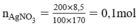
Phương trình hóa học của phản ứng:
HCl + AgNO3 → AgCl + HNO3
Theo pt nHCl = nAgCl = 0,1 mol
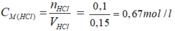
b) 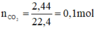
Phương trình hóa học của phản ứng:
HCl + NaHCO3 → NaCl + CO2↑ + H2O
Theo pt: nHCl = nCO2 = 0,1 mol ⇒ mHCl = 0,1. 36,5 = 3,65 g
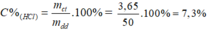

Các yếu tố ảnh hưởng đến tốc độ phản ứng là: nồng độ (càng cao tốc độ càng tăng), nhiệt độ (càng cao tốc độ càng tăng), diện tích tiếp xúc (càng cao tốc độ càng tăng), áp suất (với chất khí càng cao tốc độ càng tăng), xúc tác (luôn tăng)
Ta thấy ở thí nghiệm 2 nồng độ HCl, nhiệt độ, áp suất, xúc tác là như nhau. Diện tích tiếp xúc ở nhóm 2 nhiều hơn nhóm 1 (do bột nhỏ hơn miếng) nên nhóm 2 khí thoát ra mạnh hơn. Đáp án A.

Đáp án A
Các yếu tố ảnh hưởng đến tốc độ phản ứng là: nồng độ (càng cao tốc độ càng tăng), nhiệt độ (càng cao tốc độ càng tăng), diện tích tiếp xúc (càng cao tốc độ càng tăng), áp suất (với chất khí càng cao tốc độ càng tăng), xúc tác (luôn tăng)
Ta thấy ở thí nghiệm 2 nồng độ HCl, nhiệt độ, áp suất, xt là như nhau. Diện tích tx ở nhóm 2 nhiều hơn nhóm 1 (do bột nhỏ hơn miếng) nên nhóm 2 khí thoát ra mạnh hơn

a) HCl+ AgNO3-------->AgCl+HNO3
m AgNO3= 250.13,6/100=34(g)
m AgNO3=340170=0,2(mol)
Theo pthh
n HCl=n AgCl=0,2(mol)
CM HCl=0,2/0,3=0,667(M)
b) HCl+ NaHCO3--->NaCl+H2O+CO2
n CO2=6,72/22,4=0,3(mol)
Theo pthh
n HCl=n CO2=0,3(mol)
m HCl=0,3.36,5=10,95(g)
C% HCl=10,95/130.100%=8,42%
Chúc bạn học tốt


Chọn B
Khi tăng nồng độ chất phản ứng tốc độ phản ứng tăng
→ Cốc A xuất hiện kết tủa nhanh hơn cốc B