Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Tổng khối lượng 2 thanh kim loại sau phản ứng vẫn là 2a gam
=> mthanh 1 tăng = mthanh 2 tăng
Đặt số mol kim loại phản ứng với AgNO3 và Cu(NO3)2 lần lượt là x, y
=> 108 . 2 x - M X . x = M X . y - 64 y ( 1 )
Nồng độ mol của muối kim loại X trong dung dịch Cu(NO3)2 gấp 10 lần trong dung dịch AgNO3.
⇒ y 1 , 5 = 10 . x 0 , 1 ⇒ y = 150 x thay vào (1) được:
108 . 2 x - M X . x = M X . 150 x - 64 . 150 x ⇒ M X = 65 => X là Zn.

Đáp án D
Thanh thứ nhất giảm và thành thứ 2 tăng nên: 64 < M < 207
Chỉ có Zn (65) thỏa mãn

Đáp án C.
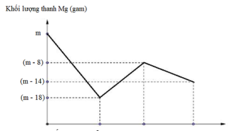
Phân tích đồ thị:
+ Đoạn 1: 3Mg + 8H+ + 2NO3- → 3Mg2+ + 2NO + 4H2O.
+ Đoạn 2: Mg + Cu2+ → Mg2+ + Cu
+ Đoạn 3: Mg + 2H+ → Mg2+ + H2
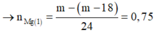
![]()
![]()
![]()

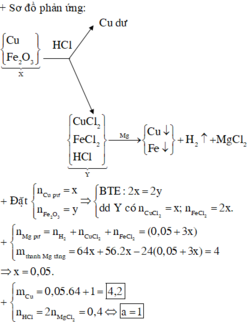
Căn cứ vào 4 đáp án: Khi M là Cu hay Fe thì kim loại chỉ tan trong dung dịch X (phản ứng với Fe3+) mà không có phần không tan tách ra, do đó phần dung dịch Y còn lại sẽ có khối lượng lớn hơn khối lượng của dung dịch X.
Do đó ta loại đáp án C và D, kim loại M là Mg hoặc Ca.
Nếu M là Ca thì
nCa dư = n H 2 = 0,28 > nCa ban đầu = 0.24
→ M là Mg
Đáp án A

Đáp án C
nHNO3 = 0,68; nNO = 0,12
nHNO3 = 4nNO+ 10nNH4NO3=> nNH4NO3 = 0,02 => ne = 3nNO + 8nNH4NO3 = 0,52
mmuối = mkim loại + 62ne + mNH4NO3=> 2,5m + 8,49 = m + 62.0,52 + 80.0,02 => m = 16,9
Bảo toàn ne=>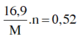 =>
=> 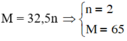
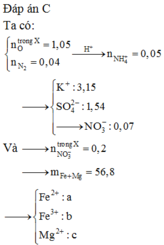



Đáp án D