Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
Gọi \(n_{Al\left(p.ứ\right)}=a\left(mol\right)\) \(\Rightarrow n_{Cu}=\dfrac{3}{2}a\left(mol\right)\)
Tăng giảm khối lượng: \(77,6-50=64\cdot\dfrac{3}{2}a-27a\)
\(\Rightarrow a=0,4\) \(\Rightarrow\left\{{}\begin{matrix}n_{Cu}=0,6\left(mol\right)\\n_{Al}=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Al\left(p.ứ\right)}=0,4\cdot27=10,8\left(g\right)\\m_{Cu}=0,6\cdot64=38,4\left(g\right)\end{matrix}\right.\)

PTHH: \(Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\)
Ta có: \(\left\{{}\begin{matrix}n_{AgNO_3\left(banđầu\right)}=0,6\cdot0,8=0,48\left(mol\right)\\n_{AgNO_3\left(saup/ư\right)}=0,6\cdot0,2=0.12\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{AgNO_3\left(pư\right)}=0,36mol\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Zn\left(pư\right)}=0,18mol\\n_{Ag}=0,36mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Zn\left(pư\right)}=0,18\cdot65=11,7\left(g\right)\\m_{Ag}=0,36\cdot108=38,52\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m=50-11,7+38,52=76,82\left(g\right)\)

Câu 1:
2M+nCuSO4\(\rightarrow\)M2(SO4)n+nCu
2M+nFeSO4\(\rightarrow\)M2(SO4)n+nFe
- Gọi a là số mol của M
- Độ tăng khối lượng PTHH1:
64na/2-Ma=20 hay(32n-M).a=20
- Độ tăng khối lượng PTHH2:
56.na/2-Ma=16 hay (28n-M)a=16
Lập tỉ số ta được:\(\dfrac{32n-M}{28n-M}=\dfrac{20}{16}=1,25\)
32n-M=35n-1,25M hay 0,25M=3n hay M=12n
n=1\(\rightarrow\)M=12(loại)
n=2\(\rightarrow\)M=24(Mg)
n=3\(\rightarrow\)M=36(loại)
Câu 2:Gọi A là khối lượng thanh R ban đầu.
R+Cu(NO3)2\(\rightarrow\)R(NO3)2+Cu
R+Pb(NO3)2\(\rightarrow\)R(NO3)2+Pb
- Gọi số mol Cu(NO3)2 và Pb(NO3)2 là x mol
- Độ giảm thanh 1: \(\dfrac{\left(R-64\right)x}{A}.100=0,2\)
- Độ tăng thanh 2: \(\dfrac{\left(207-R\right)x}{A}.100=28,4\)
Lập tỉ số: \(\dfrac{207-R}{R-64}=\dfrac{28,4}{0,2}=142\)
207-R=142R-9088 hay 143R=9295 suy ra R=65(Zn)

Vì còn Cu nên chứng tỏ Fe+3 đã bị chuyển hết thành Fe+2 rồi.
gọi x là số mol Cu+2 và 2x là số mol Fe+2
Ta dùng phương pháp tăng giảm KL
64x + 56.2x - 24.3x = m tăng
m tăng = 4 + 0,05.24 ( một phần bị axit hòa tan ) suy ra x = 0,05
Vậy khối lượng Cu ban đầu là
1 + 0,05 .64 = 4,2 g
Số Mol axit bằng
3x.2 + 2.nH2 = 0,4 mol

a)
$n_{AgNO_3\ pư} = 1.(0,5 - 0,3) = 0,2(mol)$
M + 2AgNO3 → M(NO3)2 + 2Ag
0,1.......0,2............................0,2.......(mol)
Suy ra : $0,2.108 - 0,1M = 19,2 \Rightarrow M = 24(Mg)$
Vậy M là kim loại Magie

n C u S O 4 = 0,5.0,2 = 0,1 mol
2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
2x……3x……..x……3x (Mol)
Theo bài ta có:
m C u b á m v à o - m A l tan = m A l t ă n g
⇔ 3x.64 - 2x.27 = 25,69 - 25
⇔ 138x = 0,69
⇔ x = 0,005 mol
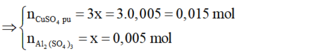

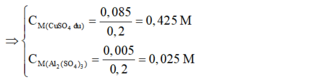
⇒ Chọn D.

PTHH: \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
x__________________x_______2x (mol)
Giả sử lượng Bạc bám hết vào thanh đồng
Ta có: \(3-64x+108\cdot2x=4,21\) \(\Rightarrow x\approx0,008\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Cu\left(p/ứ\right)}=n_{Cu\left(NO_3\right)_2}=0,008\left(mol\right)\\n_{Ag}=0,016\left(mol\right)\\\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Cu\left(p/ứ\right)}=0,008\cdot64=0,512\left(g\right)\\m_{Ag}=0,016\cdot108=1,728\left(g\right)\\m_{Cu\left(dư\right)}=2,488\left(g\right)\\m_{Cu\left(NO_3\right)_2}=0,008\cdot188=1,504\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd\left(sau.p/ứ\right)}=m_{Cu\left(ban.đầu\right)}+m_{ddAgNO_3}-m_{Ag}-m_{Cu\left(dư\right)}=228,784\left(g\right)\)
\(\Rightarrow C\%_{Cu\left(NO_3\right)_2}=\dfrac{1,504}{228,784}\cdot100\%\approx0,66\%\)
Al + 3AgNO3 → Al(NO3)3 + 3Ag
mAgNO3 = 300.17% =51 gam => nAgNO3 =51/170 = 0,3 mol
nAl = \(\dfrac{20}{27}\) mol. Ta có \(\dfrac{nAl}{1}\)>\(\dfrac{nAgNO_3}{3}\)=> Al dư , AgNO3 hết .
nAl phản ứng = 0,1 mol , nAg = 0,3 mol
Khi thanh nhôm phản ứng với muối bạc nitrat , nhôm tan ra khỏi thanh , bạc tạo thành lại bám vào thanh nhôm và lượng nhôm tan ra ít hơn lượng bạc bám vào
=> khối lượng thanh nhôm sau phản ứng = mAl ban đầu - mAl tan + mAg bám vào = 20 - 0,1.27 + 0,3.108 = 49,7 gam