Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
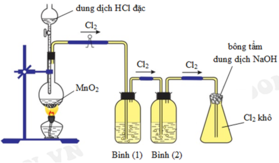
ó Giải thích sơ đồ thí nghiệm điều chế khí clo sạch trong phòng thí nghiệm:
- Phản ứng: ![]()
ó Vì dung dịch HCl dùng là đặc nên dễ bay hơi, tách ra khỏi dung dịch tạo khí HCl, H2O khi đun nóng cũng dễ bay hơi nên sản phẩm phản ứng ngoài khí Cl2 thu được còn có lẫn khí HCl và H2O.
ó Vì lẫn khí HCl và H2O nên để thu khí Cl2 sạch cần bố trí thêm 2 bình (1) và (2) để giữ lại chúng.
- Bình (1) dùng dung dịch NaCl nhằm giữ lại khí HCl, đồng thời cũng hạn chế khả năng tan của khí Cl2.
- Khí thoát ra bình (1) là Cl2 lẫn H2O nên bình (2) chứa H2SO4 đặc để giữ H2O lại.
® khí Cl2 thoát ra khỏi bình (2) được thu ở bình tam giác được nút bằng bông tẩm dung dịch NaOH.
Vì phản ứng: ![]()
nên tránh trường hợp khí Cl2 đầy bình thoát ra ngoài.
Xem xét các phát biểu:
þ (a) đúng. Với MnO2 thì cần đun nóng, còn với KMnO4 thì có thể đun hoặc không đun.
ý (b) sai. Vì nếu đổi thì lúc qua bình (1), khí Cl2 thoát ra có thể lẫn khí H2O ® không sạch nữa.
ý (c) sai. Vì bình (2) không giữ được khí HCl.
þ (d) đúng.
ý (e) sai. Vì chất rắn NaCl không giữ được khí HCl, bình (2) cũng không nên khí Cl2 thu không sạch.
® có tất cả 2 phát biểu đúng.

Đáp án B
ó Giải thích sơ đồ thí nghiệm điều chế khí clo sạch trong phòng thí nghiệm:
- Phản ứng: M n O 2 + 4 H C l → to MnCl 2 + Cl 2 ↑ + 2 H 2 O
ó Vì dung dịch HCl dùng là đặc nên dễ bay hơi, tách ra khỏi dung dịch tạo khí HCl, H2O khi đun nóng cũng dễ bay hơi nên sản phẩm phản ứng ngoài khí Cl2 thu được còn có lẫn khí HCl và H2O.
ó Vì lẫn khí HCl và H2O nên để thu khí Cl2 sạch cần bố trí thêm 2 bình (1) và (2) để giữ lại chúng.
- Bình (1) dùng dung dịch NaCl nhằm giữ lại khí HCl, đồng thời cũng hạn chế khả năng tan của khí Cl2.
- Khí thoát ra bình (1) là Cl2 lẫn H2O nên bình (2) chứa H2SO4 đặc để giữ H2O lại.
® khí Cl2 thoát ra khỏi bình (2) được thu ở bình tam giác được nút bằng bông tẩm dung dịch NaOH.
Vì phản ứng: 2 NaOH + Cl 2 → NaCl + NaClO nên tránh trường hợp khí Cl2 đầy bình thoát ra ngoài.
Xem xét các phát biểu:
þ (a) đúng. Với MnO2 thì cần đun nóng, còn với KMnO4 thì có thể đun hoặc không đun.
ý (b) sai. Vì nếu đổi thì lúc qua bình (1), khí Cl2 thoát ra có thể lẫn khí H2O ® không sạch nữa.
ý (c) sai. Vì bình (2) không giữ được khí HCl.
þ (d) đúng.
ý (e) sai. Vì chất rắn NaCl không giữ được khí HCl, bình (2) cũng không nên khí Cl2 thu không sạch.
® có tất cả 2 phát biểu đúng.

Đáp án A
Giải thích sơ đồ thí nghiệm điều chế khí clo sạch trong phòng thí nghiệm:
Phản ứng: M n O 2 + 4 H C L → t ° M n C l 2 + C l 2 ↑ + 2 H 2 O .
Vì dung dịch HCl dùng là đặc nên dễ bay hơi, tách ra khỏi dung dịch tạo khí HCl, H2O khi đun nóng cũng dễ bay hơi nên sản phẩm phản ứng ngoài khí Cl2 thu được còn có lẫn khí HCl và H2O. Vì lẫn khí HCl và H2O nên để thu khí sạch cần bố trí thêm 2 bình (1) và (2) để giữ chúng lại.
Bình (1) dùng dung dịch NaCl nhằm giữ lại khí HCl, đồng thời cũng hạn chế khả năng tan của khí Cl2.
Khí thoát ra bình (2) là Cl2 có lẫn H2O nên bình (2) chứa H2SO4 đặc để giữ H2O lại.
→ khí Cl2 thoát ra khỏi bình (2) được thu ở bình tam giác được nút bằng bông tẩm dung dịch NaOH.
Vì phản ứng: 2NaOH + Cl2 → NaCl + NaClO nên tránh trường hợp khí Cl2 đầy bình thoát ra ngoài.
Xem xét các phát biểu:
(a) đúng. Với MnO2 thì cần đun nóng, còn KMnO4 thì có thể đun nóng hoặc không đun.
(b) sai. Vì nếu đổi thì lúc qua bình (1), khí Cl2 thoát ra có thể lẫn khí H2O → không rửa sạch nữa.
(c) sai. Vì bình (2) không giữ được khí HCl.
(d) đúng.
(e) sai. Vì chất rắn NaCl không giữ được khí HCl, bình (2) cũng không nên khí Cl2 thu ,không sạch.
→ có tất cả (2) phát biểu đúng.

Đáp án A
ó Giải thích sơ đồ thí nghiệm điều chế khí clo sạch trong phòng thí nghiệm:
· Phản ứng:
![]() .
.
ê Vì dung dịch HCl dùng là đặc nên dễ bay hơi, tách ra khỏi dung dịch tạo khí HCl, H2O khi đun nóng cũng dễ bay hơi nên sản phẩm phản ứng ngoài khí Cl2 thu được còn có lẫn khí HCl và H2O.
ê Vì lẫn khí HCl và H2O nên để thu khí sạch cần bố trí thêm 2 bình (1) và (2) để giữ chúng lại.
· Bình (1) dùng dung dịch NaCl nhằm giữ lại khí HCl, đồng thời cũng hạn chế khả năng tan của khí Cl2.
· Khí thoát ra bình (2) là Cl2 có lẫn H2O nên bình (2) chứa H2SO4 đặc để giữ H2O lại.
→ khí Cl2 thoát ra khỏi bình (2) được thu ở bình tam giác được nút bằng bông tẩm dung dịch NaOH.
Vì phản ứng: 2NaOH + Cl2 → NaCl + NaClO nên tránh trường hợp khí Cl2 đầy bình thoát ra ngoài.
Xem xét các phát biểu:
þ (a) đúng. Với MnO2 thì cần đun nóng, còn KMnO4 thì có thể đun nóng hoặc không đun.
ý (b) sai. Vì nếu đổi thì lúc qua bình (1), khí Cl2 thoát ra có thể lẫn khí H2O → không rửa sạch nữa.
ý (c) sai. Vì bình (2) không giữ được khí HCl.
þ (d) đúng.
ý (e) sai. Vì chất rắn NaCl không giữ được khí HCl, bình (2) cũng không nên khí Cl2 thu ,không sạch.
→ có tất cả (2) phát biểu đúng.

Chọn A.
(a) Sai, Không thể thay dung dịch axit sunfuric đặc bằng dung dịch axit sunfuric loãng.
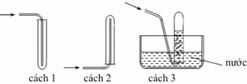
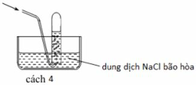
(c) Sai, Dung dịch NaCl bão hòa được thêm vào ống nghiệm để phân tách lớp sản phẩm thu được.
(d) Sai, Không thể thay dung dịch NaCl bão hòa bằng dung dịch HCl bão hòa.
(e) Sai, Để nâng cao hiệu suất của phản ứng (tức chuyển dịch cân bằng về phía tạo thành este) có thể lấy dư một trong hai chất đầu hoặc làm giảm nồng độ của sản phẩm.
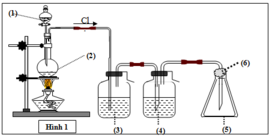




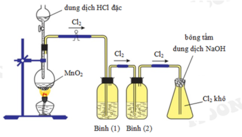
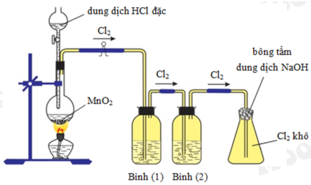

Đáp án : C
Vì khí là Cl2 cần loại bỏ HCl => (3) và (4) phải chứa dung dịch giữ lại HCl nhưng không ảnh hưởng đến Cl2