Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khi đọc lướt qua đề bài, ta nhận thấy có vẻ như cách làm của bài này cũng tương tự như bài trước là tìm mối quan hệ giữa số mol của CO2 và H2.
Do đó ta cũng sẽ đi viết công thức cấu tạo của các chất trong hỗn hợp X ban đầu:
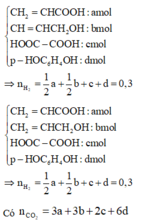
Ở đây nhận thấy ta không thể tìm ngay được mối quan hệ giữa n C O 2 và n H 2 như bài trước vì hệ số của c trong phép tính số mol CO2 là 2 mà không phải là 6.
Khi đó ta cần suy nghĩ đến một hướng làm khác khi mà bài tập không đủ dữ kiện để giải hết các nghiệm là tìm giới hạn của ẩn hoặc đại lượng nào đó.
Ta có:a + b + 2c + 2d < 3a + 3b + 2c + 6d < 3a + 3b + 6c + 6d
![]()
hay 13,44 < V < 40,32
Đáp án D.

Chọn A
Hỗn hợp X gồm 3 chất là ancol metylic, etylen glicol và glixerol, nhưng lại chỉ có một giả thiết nên coi hỗn hợp X chỉ gồm 1 chất là ancol metylic.
Theo bảo toàn nguyên tố C và bảo toàn nguyên tố H trong nhóm -OH, ta có
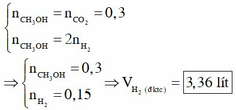

Đáp án là B
Fructozo + H2 → sobitol : C6H8(OH)6 (X)
(Y) : CH3OH , C3H5(OH)3
Nhận thấy , trong X và Y , đều có
nOH- = nC =0,25 (mol)
Khi Y tác dụng với Na dư , ta có :
n H 2 = 1 2 nOH- = 0, 125 (mol)
=> V = 2,8(l)

Đáp án B
Nhận thấy: Cứ 1 nhóm -COOH phản ứng với NaHCO3 tạo 1 phân tử CO2
Nên
![]()
Áp dụng định luật bảo toàn nguyên tố O ta có :
![]()
⇒a = 18.0,04 = 0,72(gam)
Đáp án B

Chọn đáp án A.
Quy luật chung : n O t r o n g X = n O t r o n g nhóm − C O O H = 2 n − C OO H
Bản chất phản ứng của X với NaHCO3 :
− C OO H + N a H C O 3 → − C OONa + CO 2 ↑ + H 2 O ( 1 ) m o l : 0 , 5 ← 0 , 5
Theo (1) và bảo toàn O trong hỗn hợp X, ta có : n − C O O H = n C O 2 = 0 , 5 m o l
⇒ n O t r o n g X = n O t r o n g n h ó m − C O O H = 2 n − C O O H = 1 m o l .
Áp dụng bảo toàn nguyên tố H trong phản ứng đốt cháy hỗn hợp X, ta có :
n H t r o n g X = 2 n H 2 O = 2. 14 , 4 18 = 1 , 6 m o l ⇒ n C O 2 = n C t r o n g X = 29 , 6 − 16 − 1 , 6 12 = 1 m o l ⇒ m C O 2 = 44 g a m

khi cho vào dung dịch NaHCO3 ta có PƯ trao đổi như sau:
H + HCO3 => H2O + CO2 Nên số mol của các nhóm COOH là 0,07 (mol)
Vậy số mol Oxy trong X là 0,07.2=0,14 mol
Bây giờ thì áp dụng định luật bảo toàn nguyên tố Oxy ta có:
2.nCO2 + nH2O = nO (trong X) + nO (trong O2)
=> nO(trong O2) =0,22 mol => nO2= 0,11 mol
=> V O2=0,11.22,4=2,464 (lít)

Đáp án C
n C O 2 = 0,2 mol; n H 2 = 0,05 mol → n - O H a n c o l = 0,1 mol → n C t r o n g a n c o l ≥ 0,1 mol;
n N a O H = n O t r o n g Z = 0,1 → n C m u ố i ≥ 0,1 mol.
n C t r o n g E = n C t r o n g a n c o l + n C m u ố i = n C O 2 = 0,2 mol
→ n C t r o n g a n c o l = 0,1 mol; n C m u ố i = 0,1 mol.
→ Ancol có số C = số O; muối có số C = số Na. Vậy ancol là C H 3 OH (0,1 mol); các muối là HCOONa a mol và C O O N a 2 b mol
Bảo toàn Na có: a + 2b = n N a O H = 0,1 mol (1).
m m u ố i = 6,76 gam → 68a + 134b = 6,76 gam (2)
Từ (1) và (2) có a = 0,06 và b = 0,02.
X là HCOOC H 3 0,06 mol và Y là C O O C H 3 2 0,02 mol.
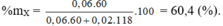

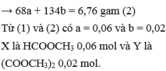
nco = 3a+ 3b+ 6c = 6d = 6^-a + -b + c + dj = 6.0,3 = l,8(mol)
Đáp án A