Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta thấy \(n_{NO3}=0,08 mol< n_{Zn}=0,09 mol=>Zn\) dư và muối trong dung dịch sau cùng là 0,04 mol Zn(NO3)2
Bảo toàn khối lượng: mZn + ,my = \(m_{dd cuối}\) +\(m_{rắn cuối}\)
=> mY = 0,04.189 + 10,53 – 5,85 = 12,24g
Bảo toàn khối lượng : mCu + mdd AgNO3 = mX + mY
=> mCu = m = 7,76 + 12,24– 0,08.170 = 6,4g.

Dung dịch muối cuối cùng là Zn(NO3)2
Ta có: nNO−3=0,4×0,2=0,08 mol
nNO3−=0,4×0,2=0,08 mol
BT: NO3-→nZn(NO3)2=0,04 mol
BTKL ba kim loại:
m + 0,4 × 0,2 × 108 + 5,85 = 7,76 + 10,53 + 0,04 × 65
→ m = 6,4 gam

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
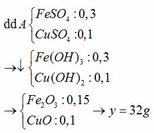

nAgNO3 = 0,12.0,25 = 0,03(mol)
PTHH: Fe + 2AgNO3 --> Fe(NO3)2 + 2Ag
_____0,015<-0,03-------------------->0,03
=> 56(x-0,015) + 0,03.108 = 3,3333
=> x = 0,01666 (mol)
=> m = 0,01666.56 = 0,93296(g)
\(Fe + 2AgNO_3 \rightarrow Fe(NO_3)_2 + 2Ag\)
Ta có:
\(n_{AgNO_3}= 0,12 . 0,25=0,03 mol\)
Theo PTHH:
\(n_{Ag}=n_{AgNO_3}= 0,03 mol\)
\(\Rightarrow m_{Ag}= 0,03 . 108= 3,24 g < 3,333g\)\(\Rightarrow m_{Fe dư}= 3,333 - 3,24 =0,093 g\)
\(n_{Fe pư}= \dfrac{1}{2} n_{AgNO_3}= 0,015 mol\)
\(\Rightarrow m= m_{Fe dư} + m_{Fe pư}= 0,015 . 56 + 0,093=0,933 g\)




\(n_{AgNO_3}=0,2.0,4=0,08\left(mol\right)\)
\(n_{Zn}=\dfrac{3,9}{65}=0,06\left(mol\right)\)
Gọi số mol Cu ban đầu là a (mol)
Gọi số mol Cu pư là b (mol)
PTHH: Cu + 2AgNO3 --> Cu(NO3)2 + 2Ag
b------>2b--------->b--------->2b
=> Rắn sau pư chứa \(\left\{{}\begin{matrix}Cu:a-b\left(mol\right)\\Ag:2b\left(mol\right)\end{matrix}\right.\)
=> 64(a - b) + 108.2b = 7
=> 64a + 152b = 7 (1)
dd sau pư chứa \(\left\{{}\begin{matrix}Cu\left(NO_3\right)_2:b\left(mol\right)\\AgNO_3:0,08-2b\left(mol\right)\end{matrix}\right.\)
- Nếu Zn tan hết:
\(n_{Zn\left(NO_3\right)_2}=n_{Zn}=0,06\left(mol\right)\)
Mà \(n_{NO_3^-}=0,08\left(mol\right)\)
=> Vô lí
=> Zn không tan hết
PTHH: Zn + 2AgNO3 --> Zn(NO3)2 + 2Ag
(0,04-b)<-(0,08-2b)------------>(0,08-2b)
Zn + Cu(NO3)2 --> Zn(NO3)2 + Cu
b<-------b--------------------->b
=> Rắn sau pư gồm \(\left\{{}\begin{matrix}Ag:0,08-2b\left(mol\right)\\Cu:b\left(mol\right)\\Zn:0,02\left(mol\right)\end{matrix}\right.\)
=> 108(0,08 - 2b) + 64b + 0,02.65 = 6,14
=> b = 0,025 (mol)
=> a = 0,05 (mol)
m = 0,05.64 = 3,2 (g)