Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích:
mO(X)=86,3.19,47/100=16,8 gam=>nO(X)=1,05 mol=>nAl2O3=nO(X)/3=0,35 mol.
nOH-=2nH2=1,2 mol.
nHCl=3,2.0,75=2,4 mol.
Al2O3+2OH-→2AlO2- +H2O
0,35 0,7 0,7(mol)
Y gồm: 0,5 mol OH- dư, 0,7 mol AlO2-
H+ + OH-→H2O
0,5←0,5 (mol)
H+ + AlO2- + H2O→Al(OH)3↓
0,7←0,7→ 0,7 (mol)
Al(OH)3↓+3H+→Al3++3H2O
0,4←2,4-0,5-0,7=1,2 (mol)
nAl(OH)3=0,7-0,4=0,3 mol =>m↓=0,3.78=23,4 g.
Đáp án A

Đáp án D
Theo đề bài ta có
![]()
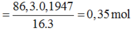
Khi hòa tan hỗn hợp X bằng nước.Xét dung dịch Y ta có :
![]()
![]()
![]()
- Khi cho dung dịch Y tác dụng với 2,4 mol HCl, vì:
![]()

![]()

Đáp án A
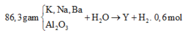
Từ số mol H2 ta tính được số mol O H - giải thích
![]()
![]()
![]() , mà
A
l
2
O
3
→
3
O
, mà
A
l
2
O
3
→
3
O
→ n A l 2 O 3 = 0 , 35 m o l
⇒ n O H - = 2 n H 2 = 1 , 2 m o l
Ta có phương trình:
![]()
=> dung dịch Y gồm

⇒ kết tủa A l ( O H ) 3
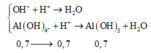
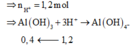
=> Số mol kết tủa còn lại là:
![]()

Đáp án B
%mO/X = 86,3×0,1947 = 16,8 gam.
⇒ nO = 1,05 ⇒ nAl2O3 = 0,35 mol.
Ta có ∑nOH– = 2nH2 = 1,2 mol.
⇒ Dung dịch Y chứa nAlO2– = nAl/Al2O3 = 0,7 mol || nOH dư = 0,5 mol.
+ Sau phản ứng trung hòa nH+ = 3,2×0,75 – 0,5 = 1,9 mol
⇒ nAl(OH)3 = 0,7 – 1 , 9 - 0 , 7 3 = 0,3 mol.
⇒ mRắn = mAl2O3 = 0 , 3 × 102 2 = 15,3 gam

mO = 86,3.19,47% = 16,8g ⇒ nO = 1,05 ⇒ nAl2O3 = 0,35
Hòa tan X vào H2O ⇒ nOH- = 2nH2 = 2.0,6 = 1,2
Al2O3 + 2OH- → 2AlO2- + H2O
0,35 → 0,7 → 0,7
⇒ nOH- còn dư = 1,2 – 0,7 = 0,5
Khi cho 2,4 mol HCl vào thì:
OH- dư + H+
→
H2O
0,5 → 0,5
AlO2- + H+ + H2O → Al(OH)3
0,7 → 0,7 → 0,7
Al(OH)3 + 3H+ → Al3+ + 3H2O
0,4 ← 1,2
⇒ nAl(OH)3 còn lại = 0,7 – 0,4 = 0,3 ⇒ mAl(OH)3 = 0,3.78 = 23,4g ⇒ Chọn D.

Đáp án A
![]()
Từ số mol H2 ta tính được số mol O H - (giải thích:
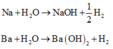
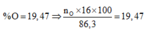
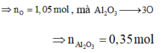
![]()
Ta có phương trình:
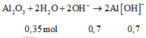
=> dung dịch Y gồm
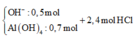
![]()
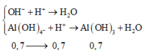
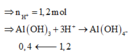
=> Số mol kết tủa còn lại là:
![]()
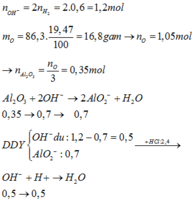
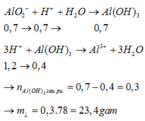
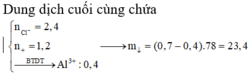
Đáp án B