Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
![]()
Khối lượng Al = 4,59 gam ® nAl = 0,17 và nAl2O3 = 0,03
Số mol NaOH phản ứng với Al3+ = 4´0,23 = 0,92 mol ® nNaOH phản ứng với NH4+ = 0,015 mol
Số mol H+ tạo thành ion NH4+ = 4´0,015 = 0,06 mol
Số mol H+ tạo H2 = 2´0,015 = 0,03 mol ® nH+ tạo H2O = 0,8 – (0,06 + 0,03) = 0,71 ® nH2O = 0,355
X + H2SO4 + NaNO3 ® Na2SO4 + Al2(SO4)3 + (NH4)2SO4 + T + H2O
0,4 0,095 0,0475 0,115 0,0075 0,355
7,65 + 0,4´98 + 0,095´85 = 0,0475´142 + 0,115´342 + 0,0075´132 + mT + 0,355´18
Khối lượng T = 1,47

Đáp án D.
![]()
![]()
- Khi cho dung dịch Z tác dụng với BaCl2 dư thì : ![]()
- Xét quá trình hỗn hợp X tác dụng với dung dịch Y ta có :
![]()
![]()
![]()
- Khi dung dịch Z tác dụng với 0,935 mol NaOH thì: ![]()
![]()
![]()
![]()
![]()
![]()

Đáp án A
nMg = 0,18 mol; nMgO = nMgCO3 = 0,06 mol. Do thu được H2 ⇒ Z không chứa NO3–.
► BaCl2 + Z → 79,22(g)↓ ⇒ ↓ là BaSO4 ⇒ nH2SO4 = nSO42– = nBaSO4 = 0,34 mol.
nNaOH phản ứng = 2nMg2+ + nNH4+ ⇒ nNH4+ = 0,01 mol. Bảo toàn điện tích: nNaNO3 = nNa+ = 0,07 mol.
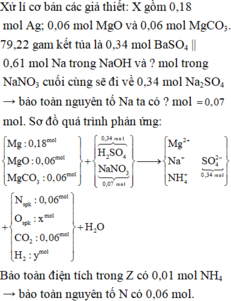
► Ta có sơ đồ quá trình sau:
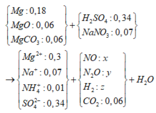
Đặt nNO = x; nN2O = y; nH2 = z. Bảo toàn nguyên tố Nitơ: x + 2y = 0,06. Bảo toàn nguyên tố Hidro:
||⇒ nH2O = (0,32 - z) mol. Bảo toàn khối lượng: 51,03 = 41,63 + 30x + 44y + 2z + 2,64 + 18 × (0,32 - z).
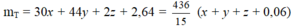
||⇒ giải hệ có: x = 0,04 mol; y = 0,01 mol; z = 0,04 mol.
⇒ nT = 0,15 mol ⇒ V = 0,15 × 22,4 = 3,36 lít


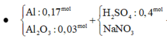
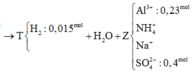
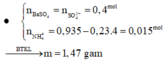



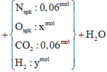



Đáp án D
+ Ta có : n Al = 0 , 17 mol ; n Al 2 O 3 = 0 , 03 mol ; n BaSO 4 = 0 , 4 mol ; n NaOH = 0 , 935 mol . + Sơ đồ phản ứng : Al Al 2 O 3 ⏟ X + H 2 SO 4 NaNO 3 ⏟ Y → NH 4 + , Al 3 + Na + , SO 4 2 - ⏟ Z + H 2 ↑ NO x ¯ ↑ ⏟ T ↓ → BaCl 2 dư BaSO 4 → NaOH pư max AlO 2 - SO 4 2 - , Na + ⏟ W + Trong W BT Al : n AlO 2 - = 0 , 23 BT S : n SO 4 2 - = 0 , 4 ⇒ BTĐT trong W : n Na + = 1 , 03 BT Na : n Na + trong Y = n Na + trong Z = 0 , 095 + BTĐT trong Z : n NH 4 + = 0 , 015 ; BT N : n NO x = 0 , 08 BT E : 3 . 0 , 17 = 0 , 08 ( 5 - 2 x ¯ ) + 0 , 015 . 2 + 0 , 015 . 8 ⇒ x ¯ = 0 , 25 m T = 1 , 47 ≈ 1 , 5 gam