Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a có:
nNO=0,05(mol) ;nH2=0,4(mol) và mZ=2,3(g)
Muối sunfat trug hòa có thể gồm FeSO4 , Fe2(SO4)3 , (NH4)2SO4, K2SO4, Al2(SO4)3
áp dụng định luật bảo toàn khối lượng
66,2 + 3,1.136=466,6+0,45.469 + mH2O → mH2O=18,9(g) → nH2O=1,05(mol)
Đặt nNH4+=x(mol). Ta có 3,1=4x+2.1,05 + 2.0,4 → x= 0,05(mol)
Vậy nNO3=0,05+0,05=0,1(mol) → nFe(NO3)2=0,05(mol)
Bảo toàn nguyên tố O ta được 4a + 0,05.6 =1,05 + 0,05
a=0,2(mol) (Với a=nFe3O4)
=>mAl =66,2-0,2.232-180.0,05 =10,8(g)
%Al = 16,1%.

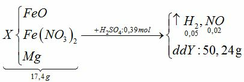
Vì Mg có tính khử rất mạnh nên trong Y có thể có muối (NH4)2SO4
BTNT N: 2nFe(NO3)2 = nNO + nNH4 => 2y = 0,02 + nNH4 => nNH4 = 2y – 0,02
BTNT H: 2nH2SO4 = 2nH2 + 4nNH4 + 2nH2O => 2 . 0,39 = 2 . 0,05 + 4 (2y – 0,02) + 2nH2O
=> nH2O = 0,38 – 4y
BTNT O: nFeO + 6nFe(NO3)2 = nNO + nH2O
=> x + 6y = 0,02 + 0,38 – 4y => x + 10y = 0,4
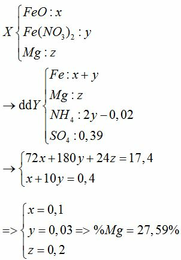

a)
2Al + 6HCl → 2AlCl3 + 3H2↑
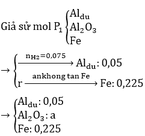
Pt: 2Al + 6H2SO4 → Al2(SO4)3 + 3SO2↑ + 6H2O
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Giả sử P2 = kP1
=> a=0.1
=> m = 128,8g
b)
2yAl + 3FexOy → yAl2O3 + 3xFe
0,1 0,225
=> 0,225y = 0,3x => 3y = 4x
=> Fe3O4





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

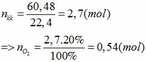
CH3OH và C2H5OH có CT chung là CnH2n+2O.
CH3OH và C2H5OH có cùng số mol nên:
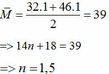
Vậy CT chung của 2 ancol là: C1,5H5O
2 axit có công thức phân tử là: C3H6O2 và C6H10O4
Nhận xét: C1,5H5O ; C3H6O2 và C6H10O4 đều có số nguyên tử C gấp 1,5 lần số nguyên tử O
Gọi số mol của CO2: x (mol) ; nH2O = y (mol)
=> nO (trong hh đầu) = 2/3 nC =2/3 nCO2 = 2x/3 (mol) ( Vì nguyên tử C gấp 1,5 lần số nguyên tử
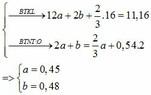
Khối lượng dung dịch giảm: ∆ = mCaCO3 – mCO2 – mH2O = 0,45.100 – 0,45.44 – 0,48.18 = 16,56 (g)

Câu 1

Áp dụng định luật bảo toàn nguyên
tố H ta có:
nHCl = 2nH2 = 2.0,045 = 0,09 mol
Áp dụng định luật bảo toàn khối lượng
ta có: mA + mHCl = m muối + mH2
=> m = m muối + mH2 – mA = 4,575 + 0,045.2 – 0,09.36,5 = 1,38 (gam)
Câu 2

Do cho kim loại phản ứng với H2SO4 đặc và HNO3 đặc nên khí sinh ra là SO2 và NO2.
Áp dụng phương pháp đường chéo ta có:
SO2: 64 4,5
50,5
NO2: 46 13,5
→nSO2=nNO2=4,513,5=13

Đặt số mol của Fe và M lần lượt là x và y (mol)
- Khi cho hỗn hợp tác dụng với HCl:
Fe + 2HCl → FeCl2 + H2
x x (mol)
M + nHCl → MCln + 0,5nH2
y 0,5ny (mol)
nH2 = 0,045 => x + 0,5ny = 0,045 (1)
- Khi cho hỗn hợp tác dụng với HNO3 đặc và H2SO4 đặc:
Ta có các bán phản ứng oxi hóa – khử:
Fe → Fe3+ + 3e
x 3x
M → Mn+ + ne
y ny
S+6 + 2e → S+4 (SO2)
0,021 0,042
N+5 + 1e → N+4 (NO2)
0,063 0,063
Áp dụng định luật bảo toàn electron ta có: 3x + ny = 0,042 + 0,063 hay 3x + ny = 0,105 (2)
Từ (1) và (2) ta có hệ phương trình sau:

Mặt khác: mA = mFe + mM => 1,38 = 0,015.56 + My => My = 0,54(4)
Từ (3) và (4) suy ra M = 9n
Ta có bảng sau:
| n |
1 |
2 |
3 |
| M |
9 (loại) |
18 (loại) |
27 (nhận) |
Vậy kim loại M là nhôm, kí hiệu là Al.
a có:
nNO=0,05(mol) ;nH2=0,4(mol) và mZ=2,3(g)
Muối sunfat trug hòa có thể gồm FeSO4 , Fe2(SO4)3 , (NH4)2SO4, K2SO4, Al2(SO4)3
áp dụng định luật bảo toàn khối lượng
66,2 + 3,1.136=466,6+0,45.469 + mH2O → mH2O=18,9(g) → nH2O=1,05(mol)
Đặt nNH4+=x(mol). Ta có 3,1=4x+2.1,05 + 2.0,4 → x= 0,05(mol)
Vậy nNO3=0,05+0,05=0,1(mol) → nFe(NO3)2=0,05(mol)
Bảo toàn nguyên tố O ta được 4a + 0,05.6 =1,05 + 0,05
a=0,2(mol) (Với a=nFe3O4)
=>mAl =66,2-0,2.232-180.0,05 =10,8(g)
%Al = 16,1%.
hòa tan hoàn toàn khối lượng Fe và Cu(tỉ lệ 1:1) bằng axit HNO3 thu được V lít hỗn hợp khí X gồm NO và NO2 và dung dịch Y (chỉ chứa 2 muốivà axit ) tỉ khối của X đối với H2 bằng 19. tính V
các bạn giải theo cách bảo toàn electron nha