Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$n_{KClO_3} = \dfrac{24,5}{122,5} = 0,2(mol)$
$n_{O_2} = \dfrac{3}{2}n_{KClO_3} = 0,3(mol)$
$V_{O_2} = 0,3.22,4 = 6,72(lít)
Đáp án B
\(KClO_3-^{t^o}\rightarrow KCl+\dfrac{3}{2}O_2\)
\(n_{O_2}=\dfrac{3}{2}n_{KClO_3}=\dfrac{3}{2}.\dfrac{24,5}{122,5}=0,3\left(mol\right)\)
=> \(V_{O_2}=0,3.22,4=6,72\left(l\right)\)
=> Chọn B

\(Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ n_{H_2}=n_{Zn}=0,1\left(mol\right);n_{HCl}=2.0,1=0,2\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\\ b,V_{ddHCl}=\dfrac{0,2}{0,5}=0,4\left(lít\right)\)

a, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{Zn}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Zn}=0,1.65=6,5\left(g\right)\)
b, \(n_{HCl}=2n_{H_2}=0,2\left(mol\right)\Rightarrow m_{ddHCl}=\dfrac{0,2.36,5}{3,65\%}=200\left(g\right)\)

\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(m_{HCl}=\dfrac{200\cdot14,6\%}{100\%}=29,2g\Rightarrow n_{HCl}=0,8mol\)
a)\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,8 0 0
0,1 0,2 0,1 0,1
0 0,6 0,1 0,1
b)Chất HCl dư và dư \(m=0,6\cdot36,5=21,9g\)
c)\(V_{H_2}=0,1\cdot22,4=2,24l\)
d)\(m_{H_2}=0,1\cdot2=0,2g\)
\(m_{ZnCl_2}=0,1\cdot136=13,6g\)
\(m_{ddZnCl_2}=6,5+200-0,2=206,3g\)
\(C\%=\dfrac{13,6}{206,3}\cdot100\%=6,59\%\)
a, ta có pt sau : Zn + 2HCl >ZnCl2 + H2 (1)
b, nHCl=\(\dfrac{200\times14,6}{100}=29,2\left(g\right)\)\(\Rightarrow n_{HCl}=\dfrac{29,2}{36,5}=0,8\left(mol\right)\)
Ta có : nZn=\(\dfrac{6,5}{65}=0,1\left(mol\right)\)
Ta có tỉ lệ số mol là : \(\dfrac{n_{Zn}}{1}< \dfrac{n_{HCl}}{2}\left(\dfrac{0,1}{1}< \dfrac{0,8}{2}\right)\)
\(\Rightarrow\) HCl dư , Zn pứ hết
Theo pt : nHClpứ = 2.nZn=2.0,1=0,2(mol)
\(\Rightarrow\)nHCl dư = nHCl bđ - nHCl pứ = 0,8 - 0,2 = 0,6 (mol)
\(\Rightarrow\)mHCl dư=0,6.36,6=21,9 (g)
c,theo pt :nH2=nZn=0,1(mol)
\(\Rightarrow\)VH2=0,1.22,4=2,24(l)
d,Các chất có trong dung dịch sau pứ là: ZnCl2 , HCl dư
mk chịu câu này ![]()

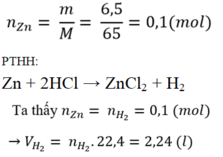
Zn+2HCl->Zncl2+H2
0,1-------------------0,1
n Zn=0,1 mol
=>VH2=0,1.22,4=2,24l
=>C
C