Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ----> ZnCl2 + H2
Mol: 0,1 0,1
b, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)

\(a.Zn+2HCl\rightarrow ZnCl_2+H_2\\ b.n_{Zn}=n_{ZnCl_2}=0,1\left(mol\right)\\ \Rightarrow m_{ZnCl_2}=0,1.136=13,6\left(g\right)\\ c.n_{H_2}=n_{Zn}=0,1\left(mol\right)\\ \Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)

a) Zn + 2HCl → ZnCl2 + H2
b) mZnCl2 = 0,1 . 136 = 13,6 gam
c) nZn = 6,5/65 = 0,1 mol . Theo tỉ lệ pư => nH2 = nZn = nZnCl2 =0,1 mol <=> VH2(đktc) = 0,1.22,4 = 2,24 lít.

a) Zn + 2HCl →ZnCl2 + H2
b) nZn = 6,5/65 = 0,1 mol . Theo tỉ lệ pư => nH2 = nZn = nZnCl2 =0,1 mol <=> VH2(đktc) = 0,1.22,4 = 2,24 lít.
c) mZnCl2 = 0,1 . 136 = 13,6 gam
d) nHCl =2nZn = 0,2 mol => mHCl = 0,2.36,5= 7,3 gam
Cách 2: áp dụng định luật BTKL => mHCl = mZnCl2 + mH2 - mZn
<=> mHCl = 13,6 + 0,1.2 - 6,5 = 7,3 gam

Theo gt ta có: $n_{Zn}=0,1(mol)$
a, $Zn+2HCl\rightarrow ZnCl_2+H_2$
b, Ta có: $n_{H_2}=0,1(mol)\Rightarrow V_{H_2}=2.24(l)$
c, Ta có: $n_{HCl}=2.n_{Zn}=0,2(mol)\Rightarrow m_{HCl}=7,3(g)$

a) PTHH: \(Zn+2HCl->ZnCl_2+H_2\)
b) Theo ĐLBTKL: \(m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\\\)
Hình như đề thiếu thì phải, nếu chỉ cho mZn thì không tính đc k/l axit clohidric cũng như tính thể tích H2. Bạn xem lại đề nha :D
số mol Zn: nZn = 26/ 65 = 0.4
a, pthh: Zn + 2HCL -> ZnCl2 + H2
theo pt: 1mol 2 mol 1mol 1mol
theo đề: 0,4 -> 0.8 -> 0.4 -> 0.4
b, khối lượng axit clohiđric tham gia pư là:
mHCl = nHCl . MHCl
= 0,4 . 36,5 = 14,6 (g)
c, Thể tích H2 thu được ở đktc là:
VH2 đktc = nH2 . 22.4
= 0.4 . 22,4 = 8,96 (lít)

\(n_{Zn}=\dfrac{3,25}{65}=0,05\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,05 0,1 0,05
b) \(n_{H2}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,05.22,4=1,12\left(l\right)\)
c) \(n_{HCl}=\dfrac{0,05.2}{1}=0,1\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddHCl}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Chúc bạn học tốt
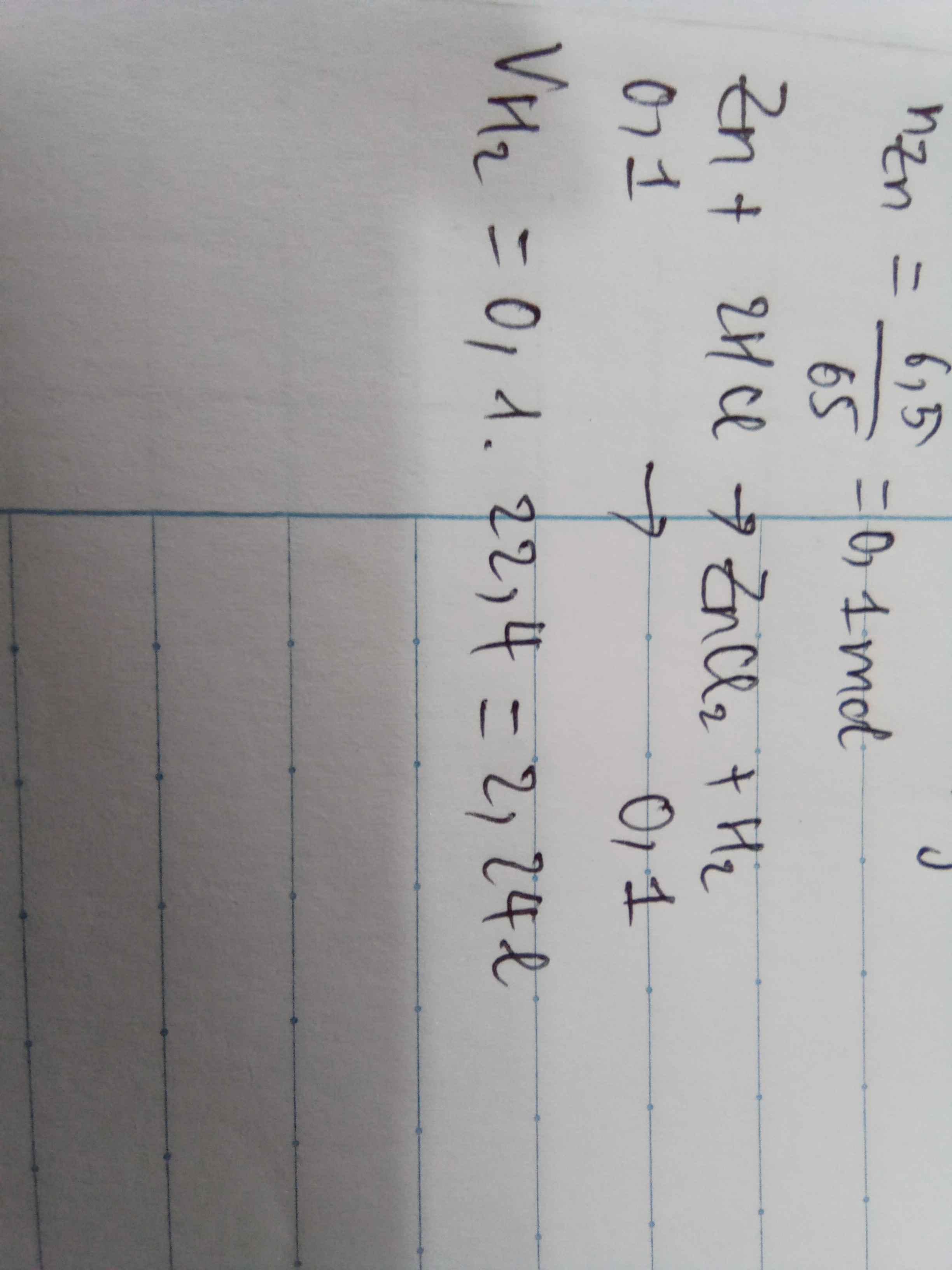
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)