Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol của BaO, BaCO3, NaHCO3 trong 30,19g hh lần lượt là x, y, z
Có 153x + 197y + 84z = 30,19
Phần 1:
BaO + H2O → Ba(OH)2
x x
OH- + HCO3- → CO32- + H2O
Ba2+ + CO32- → BaCO3
n kết tủa = 0,11
Phần 2:
BaCO3 →BaO + CO2
y y
2NaHCO3 → Na2CO3 + H2O + CO2
z z/2 z/2
=> mCO2 + mH2O = 30,19 – 26,13 = 4,06
=> 44 (y + z/2) + 18 . z/2= 4,06
TH1: Ba tạo kết tủa hoàn toàn thành BaCO3 và NaHCO3 dư
=> nBaCO3 = nBaCO3 + nBaO = 0,11 => Không thỏa mãn
TH2: Ba(OH)2 dư và NaHCO3 hết
=> x + y = 0,11 và y + z = 0,11
=> x = 0,1; y = 0,05 và z = 0,06
a.
hh Y gồm BaO: 0,15 mol; Na2CO3: 0,03 mol
BaO + H2O → Ba(OH)2
0,15 0,15
Ba(OH)2 + Na2CO3 → BaCO3 + 2NaOH
0,15 0,03 0,03 0,06
=> m kết tủa = 0,03 . 197 = 5,91g
m dd = m chất rắn + mH2O – mBaCO3 = 26,13 + 79,78 – 5,91 = 100
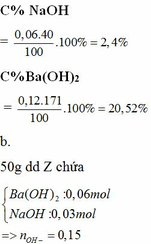
nAl2(SO4)3 = 0,02 => nAl3+ = 0,04; nSO42- = 0,06
Ba2+ + SO42- → BaSO4
0,06 0,06 0,06
nAl(OH)3 = 0,01 => mAl(OH)3 = 0,78g
m = 0,78 + 0,06 . 233 = 14,76g

Gọi $n_{Mg} = a(mol) ; n_{Fe\ pư} = b(mol) ; n_{Fe\ dư} = c(mol)$
$\Rightarrow 24a + 56b + 56c = 10,2(1)$
$Mg + CuCl_2 \to MgCl_2 + Cu$
$Fe + CuCl_2 \to FeCl_2 + Cu$
$n_{Cu} = a + b(mol)$
$\Rightarrow (a + b).64 + 56c = 13,8(2)$
$MgCl_2 + 2KOH \to Mg(OH)_2 + 2KCl$
$FeCl_2 + 2KOH \to Fe(OH)_2 + 2KCl$
$m_{kết\ tủa} = 58a + 90b = 11,1(3)$
Từ (1)(2)(3) suy ra a = 0,075 ; b = 0,075; c = 0,075
$\%m_{Mg} = \dfrac{0,075.24}{10,2}.100\% = 17,65\%$

nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
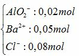 + V ml HCl 1M→ Al(OH)3: 0,01 (mol)
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)

bạn xem lại xem 13.5(g) hay 13.8g nhé ^^ ,cho tròn số ý mà
CuCl2+2NaOH->Cu(OH)2+2NaCl
nCuCl2=13.5:138=0.1(mol)
nNaOH=20:40=0.5(mol)
theo pthh:nNaOH=2nCuCl2
theo bài ra,nNaOH=5 nCuCl2->NaOH dư tính theo CuCl2
theo pthh,nCu(OH)2=nCuCl2->nCu(OH)2=0.1(mol)
mCu(OH)2=0.1*98=9.8(g)
b)PTHH:Cu(OH)2+2HCl->CuCl2+2H2O
theo pthh:nHCl=2nCu(OH)2->nHCl=0.1*2=0.2(mol)
mHCl=0.2*36.5=7.3(g)
mDD HCl=7.3*100:10=73(g)
\(a,PTHH:CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+2NaCl\\ Cu\left(OH\right)_2\rightarrow^{t^o}CuO+H_2O\)
Hiện tượng: Dung dịch màu xanh nhạt dần, xuất hiện kết tủa màu xanh lơ
Phản ứng phân hủy Cu(OH)2 sinh ra chất rắn CuO màu đen và nước
\(b,n_{CuCl_2}=\dfrac{13,5}{135}=0,1\left(mol\right)\\ m_{NaOH}=\dfrac{200\cdot2,5\%}{100\%}=5\left(g\right)\\ \Rightarrow n_{NaOH}=\dfrac{5}{40}=0,125\left(mol\right)\)
Vì \(\dfrac{n_{CuCl_2}}{1}>\dfrac{n_{NaOH}}{2}\) nên CuCl2 dư
\(\Rightarrow\dfrac{1}{2}n_{NaOH}=n_{Cu\left(OH\right)_2}=n_{CuO}=0,0625\left(mol\right)\\ \Rightarrow m=m_{CuO}=0,0625\cdot80=5\left(g\right)\)
\(c,n_{NaCl}=n_{NaOH}=0,125\left(mol\right)\\ \Rightarrow m_{NaCl}=0,125\cdot58,5=7,3125\left(g\right)\\ m_{Cu\left(OH\right)_2}=0,0625\cdot98=6,125\left(g\right)\\ \Rightarrow m_{dd_{Cu\left(OH\right)_2}}=13,5+200-7,3125=206,1875\left(g\right)\\ \Rightarrow C\%_{Cu\left(OH\right)_2}=\dfrac{6,125}{206,1875}\cdot100\%\approx2,97\%\)

Tính toán theo PTHH :
Mg + CuSO4 → Cu + MgSO4
Mg + FeSO4 → Fe + MgSO4
Ba(OH)2 + MgSO4 → BaSO4 + Mg(OH)2
Ba(OH)2 + FeSO4 → BaSO4 + Fe(OH)2
Mg(OH)2 → MgO + H2O
2 Fe(OH)2 + ½ O2 → Fe2O3 + 2 H2O
Giả sư dung dịch muối phản ứng hết
=> n Fe = n FeSO4 = 0,2 . 1= 0,2 mol => m Fe = 0,2 . 56 = 11,2 g
=> n Cu =n CuSO4 = 0,2 . 0,5 = 0,1 mol => m Cu = 0,1 . 64 = 6,4 g
=> m chất rắn = 11,2 + 6,4 = 17,6 g > 12 g > 6,4
=> kim loại Fe dư sau phản ứng Vì CuSO4 phản ứng trước sau đó mới đến FeSO4 phản ứng
CuSO4 đã hết và phản ứng với 1 phần FeSO4
12 g = m Cu + m Fe phản ứng = 6,4 g + m Fe phản ứng
=> m Fe = 5,6 g => n Fe = 0,1 mol => n FeSO4 dư = 0,2 – 0,1 = 0,1 mol
Theo PTHH : n Mg = 0,1 + 0,1 = 0,2 mol ( bắng số mol CuSO4 và FeSO4 phản ứng )
Theo PTHH : n Mg = n MgSO4 = n Mg(OH)2 = n MgO = 0,2 mol
n FeSO4 dư = n Fe(OH)2 = n Fe2O3 . 2 = 0,1 mol
=> n Fe2O3 = 0,1 mol
=> m chất rắn = m Fe2O3 + m MgO = 0,1 . 160 + 0,2 . 40 = 24 g

nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
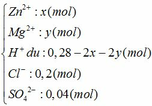
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
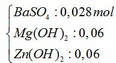
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
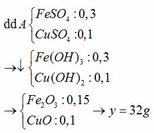

* Thí nghiệm 1: Cho hỗn hợp X tác dụng với dung dịch Br2
Đặt số mol anken A và ankin B lần lượt là x và y (mol)
nX = x + y = 0,5 (1)
CnH2n + Br2 → CnH2nBr2
x x
CmH2m-2 + 2Br2 → CmH2m-2Br4
y 2y
=> nBr2 = x + 2y = 0,8 (2)
Từ (1) và (2) ta có:
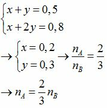
* Thí nghiệm 2: Đốt cháy hỗn hợp X
Hấp thụ CO2 vào dung dịch Ca(OH)2 thấy xuất hiện kết tủa, thêm KOH dư vào dung dịch thu được lại tiếp tục xuất hiện kết tủa nên ta có các phương trình hóa học sau:
CO2 + Ca(OH)2 → CaCO3 + H2O
0,25 ← 0,25
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,05 ← 0,025
Ca(HCO3)2 + 2KOH → K2CO3 + CaCO3 + 2H2O
0,025 ← 0,025
nCO2 = 0,25 + 0,05 = 0,3 mol
Ta có: m dung dịch giảm = mCaCO3 – mCO2 – mH2O => 7,48 = 25 – 0,3.44 – mH2O
=> mH2O = 4,32 gam => nH2O = 4,32/18 = 0,24 mol
Mặt khác, nB = nCO2 – nH2O = 0,3 – 0,24 = 0,06 mol
=> nA = 0,06(2/3) = 0,04 mol
BTNT C: nCO2 = n.nA + m.nB => 0,04n + 0,06m = 0,3
=> 2n + 3m = 15 (n≥2, m≥2)
| m |
2 |
3 |
4 |
| n |
4,5 |
3 |
1,5 |
Vậy A là C3H6 và B là C3H4
Khối lượng của hỗn hợp là: m = mC3H6 + mC3H4 = 0,04.42 + 0,06.40 = 4,08 (gam)
\(n_{Fe\left(NO_3\right)_3}=\dfrac{48,4}{242}=0,2mol\)
\(n_{NaOH}\dfrac{32}{40}=0,8mol\)
Fe(NO3)3+3NaOH\(\rightarrow\)Fe(OH)3\(\downarrow\)+NaNO3
- Tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,8}{3}\)
nên NaOH dư
\(n_{Fe\left(OH\right)_3}=n_{Fe\left(NO_3\right)_3}=0,2mol\)
mY=0,2(56+17.3)=21,4 gam
mddY=48,4+32+400-21,4=458,8 gam