Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số OXH của Fe sau khi tác dụng với dung dịch HCl là +2 còn sau khi td với Cl2 là +3
TN1
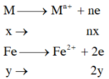
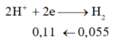
=> nx+2y=0,11 (1)
TN2: Xét cả quá trình
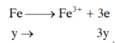
=> nx+3y=0,12 (2)
(1)-(2) được y=0,01
Thay y=0,01 vào (2) được nx=0,09(3)
Lại có: 56.0,01+ xM=1,37
=> Mx=0,81 (4)
(3)(4)=> M=9n
=> Kim loại là Al
Đáp án C

Gọi số mol Cu, M là a, b (mol)
=> 64a + b.MM = 11,2 (1)
\(n_{NO}=\dfrac{3,92}{22,4}=0,175\left(mol\right)\)
Cu0 - 2e --> Cu+2
a--->2a
M0 - ne --> M+n
b--->bn
N+5 + 3e --> N+2
0,525<-0,175
Bảo toàn e: 2a + bn = 0,525 (2)
(1)(2) => 32bn - bMM = 5,6 (3)
\(n_{H_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
PTHH: 2M + 2xHCl --> 2MClx + xH2
\(\dfrac{0,28}{x}\)<---------------------0,14
=> \(\dfrac{0,28}{x}=b\) (4)
(3)(4) => MM = 32n - 20x (g/mol)
Và \(0< x\le n\)
TH1: x = n = 1 => MM = 12 (Loại)
TH2: x = n = 2 => MM = 24 (Mg)
TH3: x = n = 3 => MM = 36 (Loại)
TH4: x = 1; n = 2 => MM = 44 (Loại)
TH5: x = 1; n = 3 => MM = 76 (Loại)
TH6: x = 2; n = 3 => MM = 56 (Fe)
Vậy M có thể là Mg hoặc Fe
=> C

Gọi a và b lần lượt là số mol của Cu và Zn
Bảo toàn khối lượng: \(m_{Cl_2}=m_{muối}-m_{hh}=8,52\left(g\right)\)
\(\Rightarrow n_{Cl_2}=\dfrac{8,52}{71}=0,12\left(mol\right)\)
Bảo toàn mol e: \(2a+2b=0,24\)
Mà \(64a+65b=7,75\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,07\end{matrix}\right.\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Theo PTHH: \(n_{H_2}=n_{Zn}=0,07mol\)
\(\Rightarrow V_{H_2}=0,07\cdot22,4=1,568\left(l\right)\)

1)
Fe + 2HCl --> FeCl2 + H2
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
2)
- Xét TN1:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,15<------------------0,15
=> mFe = 0,15.56 = 8,4 (g)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{8,4}{14,8}.100\%=56,757\%\\\%m_{Cu}=100\%-56,757\%=43,243\%\end{matrix}\right.\)
3)
- Xét TN2:
\(n_{Cu}=\dfrac{29,6.43,243\%}{64}=0,2\left(mol\right)\)
PTHH: Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,2-------------------------->0,2
=> V = 0,2.22,4 = 4,48 (l)

Các PTHH :
2Al + 3 H 2 SO 4 → Al 2 SO 4 3 + 3 H 2 (1)
2Al + 6 H 2 SO 4 → Al 2 SO 4 3 + 3 SO 2 + 6 H 2 O (2)
Cu + 2 H 2 SO 4 → Cu SO 4 + 2 H 2 O + SO 2 (3)
Theo PTHH (1) số mol Al tham gia phản ứng bằng 2/3 số mol H 2 => Khối lượng AI trong hỗn hợp : 2×2/3×0,06×27 = 2,16(g)
Số mol SO 2 được giải phóng bởi Al: 2,16/27 x 3/2 = 0,12 mol
Theo PTHH (2) và (3) số mol SO 2 giải phóng bởi Cu : 2.0,1 - 0,12 = 0,08 (mol)
Theo PTHH (3) khối lượng Cu trong hỗn hợp : 0,08. 64 = 5,12 (g)
Vậy m = 2,16 + 5,12 = 7,28 (g).




nCl2= \(\frac{3,136}{22,4}\)= 0,14 mol
\(\rightarrow\)nCl= 2nCl2= 0,28 mol
\(\rightarrow\) mCl= 9,94g
Coi X gồm M và Cl
\(\rightarrow\)mM= 22,94-9,94= 13g
1/2 hỗn hợp X gồm 13/2= 6,5g M và 9,94/2= 4,97g Cl
nH2= \(\frac{0,672}{22,4}\)= 0,03 mol
2M+ 2nHCl\(\rightarrow\)2MCln+ nH2
\(\rightarrow\) nM= \(\frac{0,06}{n}\) mol
\(\rightarrow\) MM= \(\frac{6,5n}{0,06}\)= 108n
Ko có M thoả mãn đề bài (ko thể là n=1 \(\rightarrow\) M=108 (Ag) vì Ag ko tan trong HCl)
ủa sao thầy tớ cho đáp án là Zn nhỉ ?