Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, \(\left\{{}\begin{matrix}27n_{Al}+64n_{Cu}=2,46\\3n_{Al}+2n_{Cu}=3n_{NO}=0,12\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,02\left(mol\right)\\n_{Cu}=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,54\left(g\right)\\n_{Cu}=1,92\left(g\right)\end{matrix}\right.\)
b, \(n_{HNO_3}=4n_{NO}=0,16\left(mol\right)\)
\(\Rightarrow m_{HNO_3}=10,08\left(g\right)\)
\(\Rightarrow m_{ddHNO_3}=201,6\left(g\right)\)
\(\Rightarrow m_{\text{dd sau pư}}=2,46+201,6-0,04.30=202,86\left(g\right)\)
\(\Rightarrow C\%\left(Al\left(NO_3\right)_3\right)=\dfrac{0,02.213}{202,86}.100\%=2,1\%\)
\(\Rightarrow C\%\left(Cu\left(NO_3\right)_2\right)=\dfrac{0,03.188}{202,86}.100\%=2,78\%\)

Khí không màu hóa nâu trong không khí : NO
\(n_{NO} = \dfrac{2,987}{22,4}(mol)\)
Gọi \(n_{Fe} = a(mol) ; n_{Ag} = b(mol)\\ \Rightarrow 56a + 108b = 16,4(1)\)
Bảo toàn electron :\(3n_{Fe} + n_{Ag} = 3n_{NO}\)
\(\Rightarrow 3a + b = \dfrac{2,987}{22,4}.3(2)\)
Từ (1)(2) suy ra a = 0,1 ; b = 0,1
Vậy :
\(\%m_{Fe} = \dfrac{0,1.56}{16,4}.100\% = 34,15\% \\\%m_{Ag} = 100\% - 34,15\% = 65,85\%\)

- Viết đúng ptpư:
\(Fe+4HNO_3\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\)
\(3Cu+8HNO_3\rightarrow2Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(nNO=0,04\left(mol\right)\)
Gọi nFe là x(mol) ; nCu là y(mol)
ta có hệ pt:
\(\left\{{}\begin{matrix}m_{hh}=56x+64y=3,04\\nNO=x+\dfrac{2}{3y}=0,04\end{matrix}\right.\)
Giải hệ ta được: x = 0,02 mol ; y = 0,03 mol
\(\Rightarrow mFe=0,02.56=1,12\left(g\right)\)
\(mCu=0,03.64=1,92\left(g\right)\)

a)
$Cu + 4HNO_3 \to Cu(NO_3)_2 + 2NO_2 + 2H_2O$
$Ag + 2HNO_3 \to AgNO_3 + NO_2 + H_2O$
b)
Gọi $n_{Cu} = a(mol) ; n_{Ag} = b(mol) \Rightarrow 64a + 108b = 4,52(1)$
$n_{NO_2} =2a + b = 0,07(2)$
Từ (1)(2) suy ra a = 0,02 ; b = 0,03
$\%m_{Cu} = \dfrac{0,02.64}{4,52}.100\% = 28,31\%$
$\%m_{Ag} = 71,69\%$

Đặt: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\) (x,y: nguyên, dương)
PTHH: Fe + 4 HNO3 -> Fe(NO3)3 + NO + 2 H2O
x_____________________________x(mol)
3 Cu + 8 HNO3 ->3 Cu(NO3)2 + 2 NO + 4 H2O
y_________________________2/3y(mol)
Ta có hpt: \(\left\{{}\begin{matrix}56x+64y=12,4\\x+\dfrac{2}{3}y=0,15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,15\end{matrix}\right.\)
=>mFe=0,05.56=2,8(g)
=>%mFe=(2,8/12,4).100=22,581%
=>%mCu= 77,419%

1.
a. nNO2=\(\frac{24,64}{22,4}\)=1,1mol
Al+6HNO3\(\rightarrow\)Al(NO3)3+3NO2+3H2O
Cu+4HNO3\(\rightarrow\)Cu(NO3)2+2NO2+2H2O
Gọi sô ml Al và Cu là a và b
Ta có 27a+64b=14,5(1)
Lại có nNO2=3nAl+2nNO2\(\rightarrow\)3a+2b=1,1(1)
Từ (1) và (2)
\(\left\{{}\begin{matrix}\text{ 27a+64b=14,5}\\\text{3a+2b=1,1}\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}a=0,3\\b=0,1\end{matrix}\right.\)
\(\rightarrow\)%mAl=\(\frac{\text{0,3.27}}{14,5}\)=55,86%
\(\rightarrow\)%mCu=44,14%
b. Khối lượng muối:
mAl(NO3)3+mCu(NO3)2=0,3.213+0,1.188=82,7

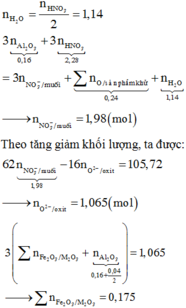
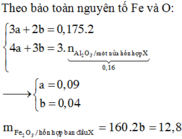
\(Đặt:\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\\ Fe\rightarrow Fe^{3+}+3e\\ Cu\rightarrow Cu^{2+}+2e\\ 4H^++NO_3^-+3e\rightarrow NO+2H_2O\\ Bảotoàne:3x+2y=0,4.3\\ Tacó:56x+64y=30,4\\ \Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=36,84\%\\\%m_{Cu}=63,16\%\end{matrix}\right.\\ n_{HNO_3}=4n_{NO}=0,4.4=1,6\left(mol\right)\\ \Rightarrow V_{HNO_3}=\dfrac{1,6}{1}=1,6\left(l\right)\\ m_{muối}=m_{Fe\left(NO_3\right)_3}+m_{Cu\left(NO_3\right)_2}=0,2.242+0,3.188=104,8\left(g\right)\)