Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

a) m rắn=4,08 gam
b) CM Cu(NO3)2 dư=0,35M; CM Fe(NO3)2=0,2M
c) V NO2=1,792 lít
Giải thích các bước giải:
Ta có: nAgNO3=0,2.0,1=0,02 mol; nCu(NO3)2=0,5.0,2=0,1 mol; nFe=2,24/56=0,04 mol
Fe + 2AgNO3 -> Fe(NO3)2 + 2Ag
Vì nAgNO3=0,02 mol; nFe =0,04 -> Fe dư -> tạo ra 0,02 mol Ag và Fe phản ứng 0,01 mol -> dư 0,03 mol
Fe + Cu(NO3)2 -> Fe(NO3)2 + Cu
Vì Cu(NO3)2=0,1 mol; nFe =0,03 mol -> Cu(NO3)2 dư =0,07 mol ; nCu=0,03 mol
Rắn thu được gồm Ag 0,02 mol và Cu 0,03 mol -> m rắn=4,08 gam
Dung dịch sau phản ứng chứa Cu(NO3)2 dư 0,07 mol và Fe(NO3)2 0,04 mol (Bảo toàn Fe)
-> CM Cu(NO3)2=0,07/0,2=0,35M; CM Fe(NO3)2=0,04/0,2=0,2M
Hòa tan rắn bằng HNO3 đặc
Ag + 2HNO3 -> AgNO3 + NO2 + H2O
Cu + 4HNO3 -> Cu(NO3)2 +2NO2 + 2H2O
-> nNO2=nAg + 2nCu=0,02+0,03.2=0,08 mol -> V NO2=0,08.22,4=1,792 lít

a) Nhận xét: 33,84g X > 16g rắn → kim loại còn dư.
Chú ý: sau một thời gian ám chỉ các chất tham gia đều dư.
Giả sử số mol của Mg, Fe lần lượt là x, y
Tăng giảm khối lượng: (64 – 24) . x + (64 – 56) . y = 38,24 – 33,84 (1)
Chất rắn bao gồm MgO: x; Fe2O3: 0,5y; CuO: a – x – y
=> 40x + 160 . 0,5y + 80(a – x – y) = 16 (2)
Từ (1) và (2) => 10a + y = 2,55
amax <=> y = 0 => amax = 0,255
b) giá trị a đạt max thì Fe chưa tham gia pứ.
Giả sử số mol Mg dư là: z (mol) 19,12g Z cho 0,48 mol SO2 → 38,24g Z cho 0,96 mol SO2
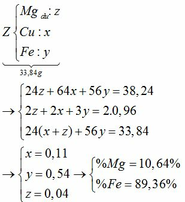

a. Các phương trình có thể xảy ra:
C + O2 → t ∘ CO2 (1)
CaCO3 → t ∘ CaO + CO2 (2)
MgCO3 → t ∘ MgO + CO2 (3)
CuCO3 → t ∘ CuO + CO2 (4)
C +CO2 → t ∘ 2CO (5)
C + 2CuO → t ∘ 2Cu + CO2 (6)
CO + CuO → t ∘ Cu + CO2 (7)
CaO + 2HCl →CaCl2 + H2O (8)
MgO + 2HCl →MgCl2 + H2O (9)
CuO + 2HCl →CuCl2 + H2O (10)
b. Vì sau phản ứng có CO và CO2, các phản ứng xảy ra hoàn toàn nên các chất còn lại sau khi nung là CaO, MgO và Cu không có phản ứng (10)
mCu = 3,2(g) => mCuCO3 = 6,2g
Gọi số mol CaCO3, MgCO3, C trong hỗn hợp lần lượt là a, b, c.(*)
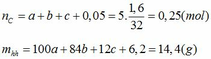
Giải ( *), (**), (***) ta được a=0,025; b=0,05; c=0,125.
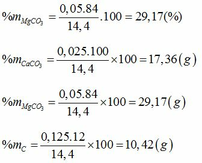



Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3

Ta có; \(\left\{{}\begin{matrix}n_{Fe}=0,04\left(mol\right)\\n_{AgNO_3}=0,02\left(mol\right)\\n_{Cu\left(NO_3\right)_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(Fe\left(0,01\right)+2AgNO_3\left(0,02\right)\rightarrow Fe\left(NO_3\right)_2\left(0,01\right)+2Ag\left(0,02\right)\)
\(Fe\left(0,03\right)+Cu\left(NO_3\right)_2\left(0,03\right)\rightarrow Fe\left(NO_3\right)_2\left(0,03\right)+Cu\left(0,03\right)\)
Dung dịch B sau phản ứng: \(\left\{{}\begin{matrix}Fe\left(NO_3\right)_2:0,01+0,03=0,04\left(mol\right)\\Cu\left(NO_3\right)_2\left(dư\right)=0,1-0,03=0,07\left(mol\right)\end{matrix}\right.\)
\(V_{ddsau}=200\left(ml\right)=0,2\left(l\right)\)
Suy ra nồng độ mol
Chất rắn A: \(\left\{{}\begin{matrix}Ag:0,02\left(mol\right)\\Cu:0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_A=0,02.108+0,03.64=4,08\left(g\right)\)
Câu này bạn tính hết số mol ra, viết pt, rồi tính theo bài toán dư hết -> đẩy số mol của chất hết sang. Giờ đang bận nên nói gọn vậy nha






a,
Fe phản ứng với AgNO3 trước Cu(NO3)2
nFe= 0,04 mol
nAgNO3= 0,02 mol
nCu(NO3)2= 0,1 mol
Fe+ 2AgNO3 \(\rightarrow\)Fe(NO3)2+ 2Ag
Spu, AgNO3 hết, dư 0,03 mol Fe, tạo ra 0,01 mol Fe(NO3)2, 0,02 mol Ag
Fe+ Cu(NO3)2 \(\rightarrow\) Fe(NO3)2+ Cu
Spu, Fe hết. Dư 0,07 mol Cu(NO3)2, tạo ra 0,03 mol Fe(NO3)2, 0,03 mol Cu
Vậy:
A chứa 0,02.108= 2,16g Ag; 0,03.64= 1,92g Cu
\(\%_{Ag}=\frac{2,16.100}{2,16+1,92}=52,94\%\)
%Cu= 47,06%
B chứa 0,01+0,03=0,04mol Fe(NO3)2, 0,07 mol Cu(NO3)2
CM Fe(NO3)2= \(\frac{0,04}{0,2}\)= 0,2M
CM Cu(NO3)2= \(\frac{0,07}{0,2}\)= 0,35M
b,
2Fe(NO3)2 \(\underrightarrow{^{to}}\) 2FeO+ 4NO2+ O2
\(\rightarrow\) Nung 0,04 mol Fe(NO3)2 tạo 0,04 mol FeO; 0,08 mol NO2; 0,02 mol O2
2Cu(NO3)2\(\underrightarrow{^{to}}\) 2CuO+ 4NO2+ O2
\(\rightarrow\) Nung 0,07 mol Cu(NO3)2 tạo 0,07 mol CuO; 0,14 mol NO2; 0,035 mol O2
m= 0,04.72+ 0,07.80= 8,48g
V= 22,4.(0,08+0,02+0,14+0,035)= 6,16l