Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tham khảo:Lấy 12,42 (g) Na2CO3.10H2O được hòa tan trong 50,1ml nước cất ( D = 1g/ml ). Tính nồng độ phần trăm của dung dịch thu đư... - Hoc24
nNa2CO3.10H2O = 12.42/286 = 0.043 (mol)
mNa2CO3 = n.M = 4.558 (g)
m nước cất = D.V = 50.1 . 1 = 50.1 (g)
mdd = 12.42 + 50.1 = 62.52 (g)
C% = 4.558x100/62.52 = 7.29 %
nNa2CO3=nNa2CO2.10H2O=12,42/286= 621/14300(mol)
\(C\%ddNa2CO3=\dfrac{\dfrac{621}{14300}.106}{12,42+50,1}.100\approx7,363\%\)

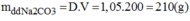
Nồng độ phần trăm của dung dịch pha chế:
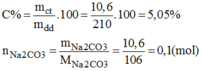
Nồng độ mol của dung dịch:
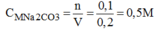

\(S_{Na_2CO_3}=\dfrac{53}{250}.100=21,2\)
\(C\%=\dfrac{53}{250+53}.100\%=17,5\%\)

\(n_{Na_2CO_3}=\dfrac{21,2}{106}=0,2\left(mol\right)\)
=> \(C_M=\dfrac{0,2}{0,3}=0,667M\)
\(m_{dd}=300.1,05=315\left(g\right)\)
=> \(C\%=\dfrac{21,2}{315}.100\%=6,73\%\)

3.
- Ta có: m dd CaCl2 = 43,8 + 156,2 = 200 (g)
Mà: C%CaCl2 = 11,1%
\(\Rightarrow\dfrac{m_{CaCl_2}}{m_{ddCaCl_2}}=0,111\) \(\Rightarrow m_{CaCl_2}=22,2\left(g\right)\) \(\Rightarrow n_{CaCl_2}=\dfrac{22,2}{111}=0,2\left(mol\right)\)
Có: \(n_{CaCl_2}=n_{CaCl_2.xH_2O}=\dfrac{43,8}{111+18x}=0,2\left(mol\right)\)
⇒ x = 6
Vậy: CTPT cần tìm là CaCl2.6H2O
- Ta có: \(n_{Na_2CO_3.xH_2O}=n_{Na_2CO_3}=0,1.0,1=0,01\left(mol\right)\)
\(\Rightarrow\dfrac{2,86}{106+18x}=0,01\)
⇒ x = 10
Vậy: CTPT cần tìm là Na2CO3.10H2O.