Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- KCl
K0-1e--> K+
Cl0+1e--> Cl-
Do 2 ion K+ và Cl- mạng điện tích trái dấu nên chúng hút nhau bởi lực hút tĩnh điện: K+ + Cl- --> KCl
- CaO
Ca0 -2e --> Ca2+
O0 +2e --> O2-
Do 2 ion Ca2+ và O2- mạng điện tích trái dấu nên chúng hút nhau bởi lực hút tĩnh điện: Ca2+ + O2- --> CaO


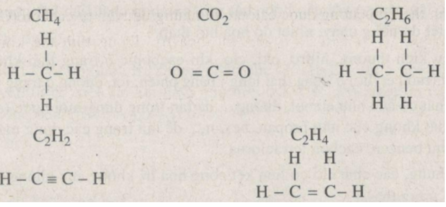
Trong các hợp chất trên, cacbon có thể tham gia 4 liên kết cộng hoá trị vì cacbon có 4 electron hoá trị, có thể góp 4 electron đó tạo thành 4 cặp electron chung.

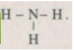
Trong phân tử NH 3 nguyên tử N tham gia 3 liên kết cộng hoá trị, vậy nitơ có cộng hoá trị 3

Bài 1.1 :
a)
Ta thấy các chất trong X đều chứa 1 pi
=> n X = n Br2 = 40/160 = 0,25(mol)
=> M X = 9,1/0,25 = 36,4
=> A là C2H4(M = 28)
Gọi n A = a(mol) ; n B = b(mol)
Ta có :
a + b = 0,25
28a + 14by = 9,1
- Nếu a = 0,25.65% = 0,1625 => b = 0,25 - 0,1625 = 0,0875
Suy ra y = 3,7
- Nếu a = 0,25.75% = 0,1875 => b = 0,25 -0,1875 = 0,0625
Suy ra y = 4,4
Với 3,7 < y < 4,4 suy ra y = 4
Vậy B là C4H8
b)
CTCT của A : CH2=CH2
$CH_2=CH_2 + HCl \to CH_2Cl-CH_3$
CTCT của B : CH3-CH=CH-CH3
$CH_3-CH=CH-CH_3 + HCl \to CH_3-CH_2-CHCl-CH_3$
Bài 1.2 :
Gọi n A = a(mol) ; n B= b(mol)
Gọi số kA = m ; kB = n(mol)
n CO2 = 15,68/22,4 = 0,7(mol) ; n H2O = 16,2/18 = 0,9(mol)
=> n CO2 - n H2O = 0,7 - 0,9 = a(m - 1) + b(n - 1)
=> am - a + bn - b = - 0,2
n pi(trong X) = n Br2 = 16/160 = 0,1(mol)
=> am + bn = 0,1
Suy ra: a + b = 0,2 + 0,1 = 0,3
Thí nghiệm 2 :
n CO2 = 20,16/22,4 = 0,9 ; n H2O = 21,6/18 = 1,2(mol)
n CO2 - n H2O = 0,9 - 1,2 = 1,5a(m -1) + b(n - 1)
=> 0,9 - 1,2 = a(m-1) + 0,5a(m-1) + b(n-1)
=> -0,3 = -0,2 + 0,5a(m-1)
=> am - a = -0,2
=>m = (a - 0,1)/a
Mà 0 < a < 0,3
=> m < 0,67
=> m = 0
Suy ra : a = 0,2 ; b = 0,3 - 0,1 = 0,1 => n = 1
Khi đốt 0,5 mol A thi thu được CO2(0,9 -0,7 = 0,2 mol)
Số nguyên tử C trong A là : 0,2/(0,2 : 2) = 2
Vậy A là C2H6
Bảo toàn nguyên tố với C
n C(trong B) = 0,7 - 0,2.2 = 0,3(mol)
=> số nguyên tử C trong B là 0,3/0,1 = 3
Vậy B là C3H6
Trong X :
m A = 0,2.28 = 5,6(gam)
m B = 0,1.42 = 4,2(gam)

Tất cả các chất trên đều tan trong nước
NaCl tan trong nước tạo thành dung dịch Natriclorua
HCl tan trong nước tạo thành dung dịch axit clohidric
$CO_2 + H_2O \rightleftharpoons H_2CO_3$
$Cl_2 + H_2O \rightleftharpoons HCl + HClO$

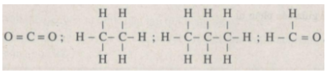

a. Công thức Lewis của CO2: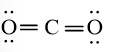
Công thức cấu tạo của CO2 là: O = C = O.
Công thức Lewis của NH3 là: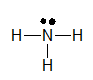
Công thức cấu tạo của NH3 là: \(H-N-H\)
\(|\)
H
b. Hợp chất tan trong nước: CO2 và NH3
Trong CO2CO2 chứa hai liên kết cộng hóa trị phân cực C=OC=O (đều phân cực về phía OO). Tuy nhiên, CO2CO2 có cấu trúc phân tử thẳng (O=C=OO=C=O) → 2 vectơ mô men cực cùng phương, ngược hướng triệt tiêu nhau → Phân tử CO2CO2 không phân cực nên có tan trong nước song là ít tan
+ NH3 tan tốt trong nước vì NH3 có liên kết cộng hóa trị phân cực trong phân tử