Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
nCl2 = 0,6 mol, nKCl = 0,5 mol
Phản ứng với KOH ở 100 độ C:
3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
0,6 mol 0,5 mol
Từ PT ⇒ Cl2 dư nên số mol KOH tính theo số mol KCl
⇒ nKOH = 0,6 mol ⇒ CM(KOH)= 0,24 M

nNaOH = 1.2,5 = 2,5 (mol)
\(n_{Cl_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2NaOH + Cl2 --> NaCl + NaClO + H2O
Xét tỉ lệ: \(\dfrac{2,5}{2}>\dfrac{0,6}{1}\) => NaOH dư, Cl2 hết
PTHH: 2NaOH + Cl2 --> NaCl + NaClO + H2O
1,2<---0,6
=> \(C_{M\left(NaOH.sau.pư\right)}=\dfrac{2,5-1,2}{2,5}=0,52M\)
=> A

Ta có :
\(n_{Cl2}=\frac{1,456}{22,4}=0,065\left(mol\right)\)
\(n_{KCl}=\frac{37,25}{74,5}=0,5\left(mol\right)\)
\(PTHH:3Cl_2+6KOH\rightarrow5KCl+KClO_3+3H_2O\)
_______0,065___0,13 ______________
\(\Rightarrow CM_{dd\left(KOH\right)}=\frac{0,13}{0,5}=0,26M\)

Cl2 + 2KOH ---> KCl + KClO + H2O
nCl2 = 0,6 mol; nKCl = 0,5 mol.
Số mol KOH = 2nKCl = 1,0 mol. Nên nồng độ KOH = 1/2,5 = 0,4M.

\(n_{KMnO_4}=\frac{15,8}{158}=0,1\left(mol\right)\)
PTHH : \(2KMnO_4+16HCl-->2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(Cl_2+H_2-as->2HCl\) (2)
Có : \(m_{ddHCl}=100\cdot1,05=105\left(g\right)\)
=> \(m_{HCl}=105-97,7=7,3\left(g\right)\)
=> \(n_{HCl}=\frac{7,3}{36,5}=0,2\left(mol\right)\)
BT Clo : \(n_{Cl_2}=\frac{1}{2}n_{HCl}=0,1\left(mol\right)\)
Mà theo lí thuyết : \(n_{Cl_2}=\frac{5}{2}n_{KMnO_4}=0,25\left(mol\right)\)
=> \(H\%=\frac{0,1}{0,25}\cdot100\%=40\%\)
Vì spu nổ thu được hh hai chất khí => \(\hept{\begin{cases}H_2\\HCl\end{cases}}\) (Vì H2 dư)
=> \(n_{hh}=\frac{13,44}{22,4}=0,6\left(mol\right)\)
=> \(n_{H_2\left(spu\right)}=n_{hh}-n_{HCl\left(spu\right)}=0,6-0,2=0,4\left(mol\right)\)
BT Hidro : \(\Sigma_{n_{H2\left(trong.binh\right)}}=n_{H_2\left(spu\right)}+\frac{1}{2}n_{HCl}=0,4+0,1=0,5\left(mol\right)\)
đọc thiếu đề câu a wtf
\(C_{M\left(HCl\right)}=\frac{0,2}{0,1}=2\left(M\right)\)

\(n_K=\dfrac{5,85}{39}=0,15\left(mol\right)\)
PTHH: 2K + 2H2O --> 2KOH + H2
_____0,15------------->0,15-->0,075
=> VH2 = 0,075.22,4 =1,68(l)
mdd = 5,85 + 100 - 0,075.2 = 105,7(g)
=> \(C\%=\dfrac{0,15.56}{105,7}.100\%=7,95\%\)
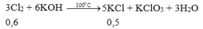


Đáp án A