Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)\(n_{CuSO_4}=0,4.0,5=0,2\left(mol\right)\)
\(PTHH:CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
Mol: 0,2 0,4 0,2
⇒ \(m_{Cu\left(OH\right)_2}=0,2.98=19,6\left(g\right)\)
b)\(C_{M\left(ddNaOH\right)}=\dfrac{0,4}{0,3}=1,3\left(M\right)\)
c)\(PTHH:Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
Mol: 0,2 0,2
=> mCuO = 0,2.80 = 16 (g)

Bài 7 :
200ml = 0,2l
\(n_{CuCl2}=2.0,2=0,4\left(mol\right)\)
Pt : \(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl|\)
1 2 1 2
0,4 0,8 0,4 0,8
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O|\)
1 1 1
0,4 0,4
a) \(n_{CuO}=\dfrac{0,4.1}{1}=0,4\left(mol\right)\)
⇒ \(m_{CuO}=0,4.40=32\left(g\right)\)
b) \(n_{NaCl}=\dfrac{0,4.2}{1}=0,8\left(mol\right)\)
⇒ \(m_{NaCl}=0,8.58,5=46,8\left(g\right)\)
\(m_{ddCuCl2}=1,35.200=270\left(g\right)\)
\(m_{ddspu}=270+100=370\left(g\right)\)
\(C_{NaCl}=\dfrac{46,8.100}{370}=12,65\)0/0
Chúc bạn học tốt

a)
$FeCl_3 + 3NaOH \to Fe(OH)_3 + 3NaCl$
$2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$
$n_{FeCl_3} = 0,3.2 = 0,6(mol)$
Theo PTHH : $n_{Fe_2O_3} = \dfrac{1}{2}n_{FeCl_3} = 0,3(mol)$
$\Rightarrow m_{Fe_2O_3} = 0,3.160 = 48(gam)$
b) Sau phản ứng, $V_{dd} = 0,3 + 0,3 = 0,6(lít)$
$n_{NaCl} = 3n_{FeCl_3} = 1,8(mol) \Rightarrow C_{M_{NaCl}} = \dfrac{1,8}{0,6} = 3M$

nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
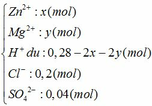
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
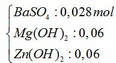
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam

\(a.CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\\ Cu\left(OH\right)_2-^{t^o}\rightarrow CuO+H_2O\\b. n_{CuSO_4}=n_{Na_2SO_4}=0,2\left(mol\right)\\ m_{Na_2SO_4}=0,2.142=28,4\left(g\right)\\ c.BTNT\left(Cu\right):n_{CuO}=n_{CuSO_4}=0,2\left(mol\right)\\ \Rightarrow m_{CuO}=0,2.80=16\left(g\right)\)

\(n_{CuSO_4}=0,5mol\)
\(n_{KOH}=0,3mol\)
a) \(CuSO_4+2KOH\rightarrow Cu\left(OH\right)_2+K_2SO_4\)
0,5 0,3 0,3 0,3
\(Cu\left(OH\right)_2\underrightarrow{t^O}CuO+H_2O\)
0,3 0,3
b)\(m_{CuO}=0,3\cdot80=24\left(g\right)\)
c) \(m_{K_2SO_4}=0,3\cdot174=52,2\left(g\right)\)
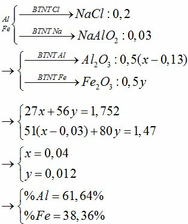
\(n_{FeCl_2}=0,1\times1=0,1\left(mol\right)\)
\(n_{NaOH}=0,3\times2=0,6\left(mol\right)\)
PTHH: FeCl2 + 2NaOH → 2NaCl + Fe(OH)2↓ (1)
Ban đầu: 0,1............0,6............................................... (mol)
Phản ứng: 0,1...........0,2................................................ (mol)
Sau pứ : 0............0,4..........→....0,2............0,1......... (mol)
a) \(m_{Fe\left(OH\right)_2}=0,1\times90=9\left(g\right)\)
Fe(OH)2 \(\underrightarrow{to}\) FeO + H2O (2)
4FeO + O2 \(\underrightarrow{to}\) 2Fe2O3 (3)
Theo Pt2: \(n_{FeO}=n_{Fe\left(OH\right)_2}=0,1\left(mol\right)\)
Theo PT3: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{FeO}=\dfrac{1}{2}\times0,1=0,05\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,05\times160=8\left(g\right)\)
b) Chất tan trong dung dịch nước lọc: NaCl và NaOH dư
\(V_{dd}saupư=100+300=400\left(ml\right)=0,4\left(l\right)\)
\(\Rightarrow C_{M_{NaCl}}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
\(C_{M_{NaOH}}dư=\dfrac{0,4}{0,4}=1\left(M\right)\)
Cảm ơn bạn nhiều lắm!!.
Mà cho mình hỏi là phải tính Fe2O3 hả bạn, tại s v? Tính feo đc k?