Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. PTHH:
CuO + HCl ---x--->
Al2O3 + 6HCl ---> 2AlCl3 + 3H2O
b. Đổi 100ml = 0,1 lít
Ta có: \(n_{HCl}=7.0,1=0,7\left(mol\right)\)
Theo PT: \(n_{Al_2O_3}=\dfrac{1}{6}.n_{HCl}=\dfrac{1}{6}.0,7=\dfrac{7}{60}\left(mol\right)\)
=> \(m_{Al_2O_3}=\dfrac{7}{60}.102=11,9\left(g\right)\)
=> \(m_{CuO}=21,1-11,9=9,2\left(g\right)\)
Sửa:
a. PTHH:
CuO + 2HCl ------> CuCl2 + H2O (1)
Al2O3 + 6HCl ---> 2AlCl3 + 3H2O (2)
b. Đổi 100ml = 0,1 lít
Ta có: \(n_{HCl}=7.0,1=0,7\left(mol\right)\)
Gọi x, y lần lượt là số mol của CuO và Al2O3
Theo PT(1): \(n_{HCl}=2.n_{CuO}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=6.n_{Al_2O_3}=6y\left(mol\right)\)
=> 2x + 6y = 0,7 (*)
Theo đề, ta có: 80x + 102y = 21,1 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+6y=0,7\\80x+102y=21,1\end{matrix}\right.\)
=> x = 0,2, y = 0,05
=> \(m_{CuO}=80.0,2=16\left(g\right)\)
\(m_{Al_2O_3}=21,1-16=5,1\left(g\right)\)

Đổi 200ml = 0,2 lít
Ta có: \(n_{HCl}=3,5.0,2=0,7\left(mol\right)\)
Gọi x, y lần lượt là số mol của CuO và Fe2O3
PTHH:
CuO + 2HCl ----> CuCl2 + H2O (1)
Fe2O3 + 6HCl ---> 2FeCl3 + 3H2O (2)
Theo PT(1): \(n_{HCl}=2.n_{CuO}=2x\left(mol\right)\)
Theo PT(2): \(n_{HCl}=6.n_{Fe_2O_3}=6y\left(mol\right)\)
=> 2x + 6y = 0,7 (*)
Theo đề, ta có: 80x + 160y = 20 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}2x+6y=0,7\\80x+160y=20\end{matrix}\right.\)
=> x = 0,05, y = 0,1
=> \(m_{CuO}=80.0,05=4\left(g\right)\)
\(m_{Fe_2O_3}=20-4=16\left(g\right)\)
đổi 200ml = 0.2 l
nhcl = 0.2*3.5 = 0.7 ( mol)
gọi số mol của CuO là x
số mol của Fe2O3 là y
PTHH:
CuO + 2HCl ➜ CuCl2 + H2O
x 2x
Fe2O3 + 6HCl ➜ 2FeCl3 + 3H2O
y 6y
ta có hệ phương trình
\(\left\{{}\begin{matrix}80x+160y=20\\2x+6y=0,7\end{matrix}\right.\)
⇒ x= 0.05
y=0.1
mCuO= 0.05*80=4 (g)
mFe2O3= 0.1*160=16(g)

CuO+2HCl--->CuCl2+H2O
x 2x x x
Fe2O3+6HCl--->2FeCl3+3H2O
y 6y 2y 3y
nHCl=3,5.0,2=0,7 mol
gọi x y lần lượt là nCuO,nFe2O3
ta có x.80+y.160=20
2x+6y=0,7 giải hệ pt ta có x=0,05 y=0,1
mCuO=0,05.80=4g
mFe2O3=0,1.160=16g
%mCuO=4/20 .100%=20%
%mFe2O3=100%-20%=80%

Gọi x,y lần lượt là số mol Al2O3, CuO
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
CuO + H2SO4 → H2O + CuSO4
\(\left\{{}\begin{matrix}102x+80y=12,3\\3x+y=\dfrac{100.24,5\%}{98}=0,25\end{matrix}\right.\)
=> x= 0,056; y=0,082
=> \(\%m_{Al_2O_3}=\dfrac{0,056.102}{12,3}.100=46,44\%\)
=> %mCuO= 100 - 46,44= 53,56%
b)
Al2O3 + 6HCl → 2AlCl3 + 3H2O
CuO + 2HCl → CuCl2 + H2O
=> \(m_{HCl}=\dfrac{(0,056.6+0,082.2).36,5}{7\%}=260,7\%\)

CuO + 2HCl -> CuCl2 + H2O (1)
Fe2O3 + 6HCl -> 2FeCl3 + 3H2O (2)
nHCl=0,2.3,5=0,7(mol)
Đặt nCuO=a
nFe2O3=b
Ta có hệ:
80a+160b=20
2a+6b=0,7
=>a=0,05;b=0,1
mCuO=80.0,05=4(g)
mFe2O3=20-4=16(g)
Theo PTHH 1 và 2 ta có:
nCuCl2=nCuO=0,05(mol)
nFeCl3=2nFe2O3=0,2(mol)
mCuCl2=135.0,05=6,75(g)
mFeCl3=162,5.0,2=32,5(g)
mdd =20+200.1,1=240(g)
C% dd CuCl2=6,72\240 .100%=2,8125%
C% dd FeCl3= 32,5\240 .100%=13,54%

Câu 3:
Gọi x, y lần lượt là số mol của MgO và Al2O3
Ta có: \(n_{H_2SO_4}=0,2.250:1000=0,05\left(mol\right)\)
a. PTHH:
MgO + H2SO4 ---> MgSO4 + H2O (1)
Al2O3 + 3H2SO4 ---> Al2(SO4)3 + 3H2O (2)
b. Theo PT(1): \(n_{H_2SO_4}=n_{MgO}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2SO_4}=3.n_{Al_2O_3}=3y\left(mol\right)\)
=> x + 3y = 0,05 (1)
Theo đề, ta có: 40x + 102y = 1,82 (2)
Từ (1) và (2), ta có HPT:
\(\left\{{}\begin{matrix}x+3y=0,05\\40x+102y=1,82\end{matrix}\right.\)
=> x = 0,02, y = 0,01
=> \(m_{MgO}=0,02.40=0,8\left(mol\right)\)
=> \(\%_{m_{MgO}}=\dfrac{0,8}{1,82}.100\%=43,96\%\)
\(\%_{m_{Al_2O_3}}=100\%-43,96\%=56,04\%\)
Câu 4:
Ta có: \(m_{H_2SO_4}=\dfrac{19,6\%.100\%}{100}=19,6\left(g\right)\)
=> \(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\left(mol\right)\)
Ta lại có: \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
a. PTHH: CuO + H2SO4 ---> CuSO4 + H2O
Ta thấy: \(\dfrac{0,1}{1}< \dfrac{0,2}{1}\)
Vậy H2SO4 dư.
Theo PT: \(n_{CuSO_4}=n_{CuO}=0,1\left(mol\right)\)
=> \(m_{CuSO_4}=0,1.160=16\left(g\right)\)
Ta có: \(m_{dd_{CuSO_4}}=8+100=108\left(g\right)\)
=> \(C_{\%_{CuSO_4}}=\dfrac{16}{108}.100\%=14,81\%\)
Câu 5: Thiếu đề
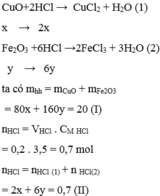
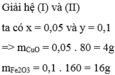
\(n_{HCl}=0,1.7=0,7\left(mol\right)\\ Đặt:n_{CuO}=a\left(mol\right);n_{Al_2O_3}=b\left(mol\right)\\ CuO+2HCl\rightarrow CuCl_2+H_2O\\ Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\\ \Rightarrow\left\{{}\begin{matrix}80a+102b=21,1\\2a+6b=0,7\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,05\end{matrix}\right.\\ \Rightarrow\%m_{CuO}=\dfrac{0,2.80}{21,1}.100\approx75,829\%\\ \Rightarrow\%m_{Al_2O_3}\approx24,171\%\)
100ml=0,1l
\(n_{HCl}=CM.V_{dd}\)=7.0,1=0,7(mol)
gọi x,y lần lượt là số mol của\(CuO\) và\(Al_2O_3\)
PTHH1:\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
x 2x x x
PTHH2:\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
y 6y 2y 3y
ta có hệ pt:\(\left\{{}\begin{matrix}m_{CuO}+m_{Al_2O_3}=21,1\left(g\right)\\n_{HCl\left(1\right)}+n_{HCl\left(2\right)}=0,7\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}80x+102y=21,1\left(g\right)\\2x+6y=0,7\left(mol\right)\end{matrix}\right.\)
giải ra ta được:x=0,2;y=0,05
\(m_{CuO}=n.M\)=0,2.80=16(g)
\(m_{Al_2O_3}=n.M\)=0,05.102=5,1(g)