Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
nOH-= 2nH2= 1,2 mol
ð nH+= 1,2 mol
Gọi thể tích dung dịch axit là x (lít)
nH+= 0,5.2x+x = 2x
ð 2x=1,2
ð x=0,6

Đáp án D
Trong dung dịch axit, ta có :
n Cl - = n HCl = 0 , 3 mol
n SO 4 2 - = n H 2 SO 4 = 0 , 15 mol
Sơ đồ phản ứng :

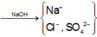
Cho NaOH vào X để thu được kết tủa lớn nhất thì dung dịch sau phản ứng chỉ còn các ion Na + , Cl - và SO 4 2 - .
Áp dụng bảo toàn điện tích trong dung dịch sau phản ứng và bảo toàn nguyên tố Na, ta có :
n NaOH = n Na + = n Cl - + 2 n SO 4 2 - = 0,6 mol
→ V dd NaOH 1 M = 0,6 lit = 600ml

$n_{HNO_3} = 0,3.1 = 0,3(mol)$
$n_{NO_2} = \dfrac{1,12}{22,4} = 0,05(mol)$
$2H^+ + NO_3^- + 1e \to NO_2 + H_2O$
$n_{HNO_3\ pư} = n_{H^+} = 2n_{NO_2} = 0,1(mol)$
$\Rightarrow n_{HNO_3\ dư} = 0,3 - 0,1 = 0,2(mol)$
Gọi $V_{dd\ B} = x(lít) \Rightarrow n_{NaOH} = 0,01x(mol) ; n_{Ba(OH)_2} = 0,02x(mol)$
mà: $n_{HNO_3\ dư} = n_{NaOH} + 2n_{Ba(OH)_2}$
$\Rightarrow 0,2 = 0,01x + 0,02x.2$
$\Rightarrow x = 4(lít)$

Đáp án D
nH2 = 3,36 : 22,4 = 0,15 (mol)
=> nOH- = 2nH2 = 0,3 (mol)
H+ + OH- → H2O
nH + = nOH - = 0,3 (mol)
Mặt khác: nH+ = nHCl + 2nH2SO4 = V + 2V = 3V (mol)
=> 3V = 0,3 => V =0,1 (lít) = 100 (ml)

Giải thích:
nH2 = 3,36 : 22,4 = 0,15 (mol)
=> nOH- = 2nH2 = 0,3 (mol)
H+ + OH- → H2O
nH + = nOH - = 0,3 (mol)
Mặt khác: nH+ = nHCl + 2nH2SO4 = V + 2V = 3V (mol)
=> 3V = 0,3 => V =0,1 (lít) = 100 (ml)
Đáp án D

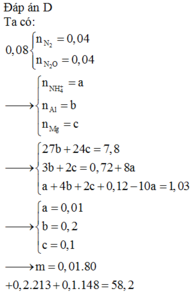
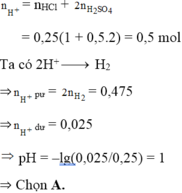
Đáp án A.
Xác định H +