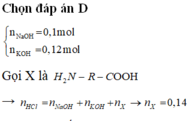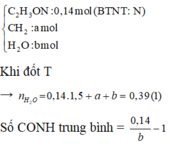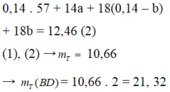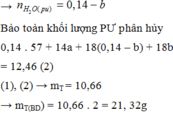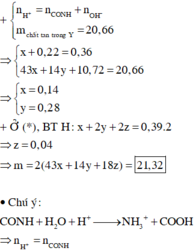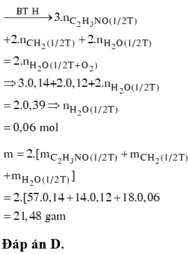Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

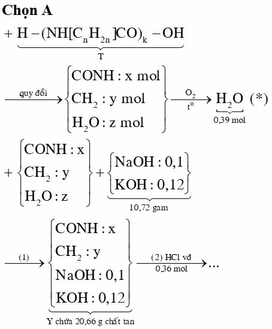
Chọn A.
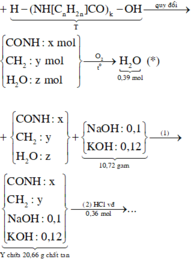
Xét hỗn hợp X ta có: n X = n H C l - n O H - = 0 , 5 m o l . Đặt CTTQ của X là CnH2n+1O2N. và mX + mNaOH = mc.tan + m H 2 O (với n H 2 O = 0 , 5 m o l ) Þ mX = 50,1 gam Þ n = 3,8
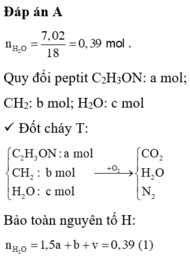
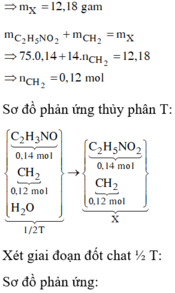
Quy đổi hỗn hợp T thành CnH2n-1ON (0,5 mol), H2O (x mol).
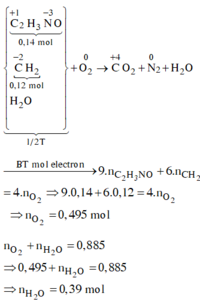
Đốt cháy T thu được: n H 2 O = n - 0 , 5 . 0 , 5 + x = 1 , 75 ⇒ x = 0 , 1 . Vậy mE = 2m = 85,8 (g)