Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp B
Phần 1: n A g = 108 108 = 1 m o l
Trường hợp 1: Hỗn hợp anđehit không chứa HCHO.
n X = 1 2 n A g = 0 , 5 m o l ⇒ M ¯ X = 10 , 4 0 , 5 = 20 , 8 < M H C H O . Loại.
Trường hợp 2: Hỗn hợp anđehit là HCHO (y mol) và CH3CHO (z mol)
⇒ 30 y + 44 z = 10 , 4 g 4 y + 2 z = 1 m o l ⇒ y = 0 , 2 z = 0 , 1
Giả sử hiệu suất tạo ete của Y là H%
Số mol H2O tạo thành 1 2 n a n c o l = 0 , 2 H % + 0 , 1.0 , 5 2 = 0 , 1 H % + 0 , 025
Áp dụng định luật bảo toàn khối lượng có:
32.0,2H% + 46.0,1.0,5 = 4,52 +18.(0,1H% + 0,025)
⇒ H% = 58,04%

Đặt công thức trung bình 2 ancol là CnH2n+1OH, công thức trung bình 3 ete là (CnH2n+1)2O, phân tử khối trung bình 3 ete là 6,76/0,08 = 84,5. Do đó: 28n + 18 = 84,5 suy ra n = 2,375. Vì vậy, 2 ancol cần tìm là C2H5OH (a mol) và C3H7OH (b mol).
Để đốt cháy hoàn toàn Z cần một lượng O2 đúng bằng lượng cần dùng để đốt cháy T:
C2H6O + 3O2 \(\rightarrow\) 2CO2 + 3H2O
C3H8O + 9/2O2 \(\rightarrow\) 3CO2 + 4H2O
Nên ta có: 40a + 60b = 27,2 và 3a + 4,5b = 43,68/22,4 = 1,95. Tính được: a = 0,2 và b = 0,3 mol.
Gọi x, y tương ứng là số mol ancol tạo ete, ta có: x + y = 2.0,08 = 0,16 và 46x + 60y = 6,76 + 18.0,02 = 8,2.
Thu được: x = 0,1 và y = 0,06 mol.
Do đó, hiệu suất tạo ete của X = 0,1/0,2 = 50%; của Y = 0,06/0,3 = 20%.

Đáp án C
Chọn đáp án C
Từ phản ứng đốt cháy hỗn hợp A:
nCO2 = 0,17 mol < nH2O = 0,25 mol ⇒ 2 ancol no, đơn chức, mạch hở.
Đặt ∑nancol = x; neste = y ⇒ nX = x + y = 0,1 mol.
► Bảo toàn nguyên tố Oxi:
⇒ nO/X = 0,13 mol = x + 4y ||⇒ giải hệ có: x = 0,09 mol; y = 0,01 mol.
► Bảo toàn khối lượng: mX = 7,48 + 4,5 - 0,23 × 32 = 4,62(g).
Thí nghiệm 1 dùng gấp 18,48 ÷ 4,62 = 4 lần thí nghiệm 2.
Trở lại thí nghiệm 1. Thuỷ phân
● 18,48(g) X chứa 0,36 mol hỗn hợp ancol và 0,04 mol este.
⇒ nNaOH phản ứng = 0,04 × 2 = 0,08 mol. Bảo toàn khối lượng:
mY = 18,48 + 0,08 × 40 - 5,36 = 16,32(g) || nY = 0,36 + 0,04 × 2 = 0,44 mol.
Lại có: 2 ancol → 1 ete + 1 H2O ||⇒ nH2O = 0,44 ÷ 2 = 0,22 mol.
► Bảo toàn khối lượng: m = 0,8 × (16,32 - 0,22 × 18) = 9,888(g) ≈ 10 gam

Đáp án C
Chọn đáp án C
Từ phản ứng đốt cháy hỗn hợp A:
nCO2 = 0,17 mol < nH2O = 0,25 mol ⇒ 2 ancol no, đơn chức, mạch hở.
Đặt ∑nancol = x; neste = y ⇒ nX = x + y = 0,1 mol.
Bảo toàn nguyên tố Oxi:
⇒ nO/X = 0,13 mol = x + 4y ||⇒ giải hệ có: x = 0,09 mol; y = 0,01 mol.
► Bảo toàn khối lượng: mX = 7,48 + 4,5 - 0,23 × 32 = 4,62(g).
Thí nghiệm 1 dùng gấp 18,48 ÷ 4,62 = 4 lần thí nghiệm 2.
Trở lại thí nghiệm 1. Thuỷ phân
● 18,48(g) X chứa 0,36 mol hỗn hợp ancol và 0,04 mol este.
⇒ nNaOH phản ứng = 0,04 × 2 = 0,08 mol. Bảo toàn khối lượng:
mY = 18,48 + 0,08 × 40 - 5,36 = 16,32(g) || nY = 0,36 + 0,04 × 2 = 0,44 mol.
Lại có: 2 ancol → 1 ete + 1 H2O ||⇒ nH2O = 0,44 ÷ 2 = 0,22 mol.
► Bảo toàn khối lượng: m = 0,8 × (16,32 - 0,22 × 18) = 9,888(g) ≈ 10 gam

Gọi công thức phân tử trung bình của X và Y là:
![]()
Đốt cháy anken:
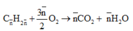
Ta có:
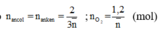
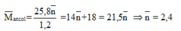
Vậy 2 ancol là:
![]()
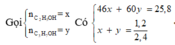
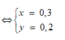
Gọi h là hiệu suất, luôn có:
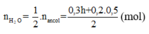
Áp dụng định luật bảo toàn khối lượng:
mancol phản ứng = m e t e + m H 2 O
⇒ 46.0,3h + 60.0,1 = 11,76 +18. 0 , 3 h + 0 , 2 . 0 , 5 2
⇒ h = 60%
Đáp án C

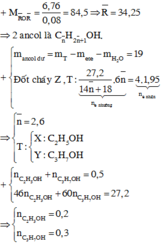


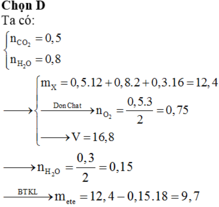
Chọn đáp án C.
n C O 2 = 5 , 6 22 , 4 = 0 , 25 m o l , n H 2 O = 6 , 3 18 = 0 , 35 m o l > n C O 2
⇒ Ancol no, đơn chức, n a n c o l = n H 2 O − n C O 2 = 0 , 35 − 0 , 25 = 0 , 1 m o l
⇒ Số nguyên tử C trung bình = n C O 2 n a n c o l = 0 , 25 0 , 1 = 2 , 5
⇒ X là C2H5OH, Y là C3H7OH
Vì 2 ancol liên tiếp nhau trong dãy đồng đẳng nên: n X = n Y = 0 , 1 2 = 0 , 05 m o l
Số mol ancol tham gia phản ứng ete hóa = 2 n e t e = 2. 0 , 42 28 = 0 , 03 m o l
Giả sử số mol X, Y tham gia phản ứng ete hóa lần lượt là x,y.
⇒ x + y = 2 n e t e = 2. 0 , 42 28 = 0 , 03 m o l 46 x + 60 y = 1 , 25 + 18.0 , 5.0 , 03 = 1 , 52 g ⇒ x = 0 , 02 y = 0 , 01
⇒ Hiệu suất tham gia phản ứng ete hóa của X = 0 , 02 0 , 05 .100 % = 40 %
Hiệu suất tham gia phản ứng ete hóa của Y = 0 , 01 0 , 05 .100 % = 20 %