Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_X=64a+56b=16.2\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
Bảo toàn e :
\(2a+3b=0.4\cdot2=0.8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.0475,b=0.235\)
\(\%Cu=\dfrac{0.0475\cdot64}{16.2}\cdot100\%=18.76\%\)
\(\%Fe=81.24\%\)
\(b.\)
\(\dfrac{a}{b}=\dfrac{0.0475}{0.235}=\dfrac{19}{94}\)
\(\Rightarrow n_{Cu}=19x\left(mol\right),n_{Fe}=94x\left(mol\right)\)
\(m_X=19x\cdot64+94x\cdot56=22\left(g\right)\)
\(\Rightarrow x=\dfrac{11}{3240}\)
\(n_{H_2}=n_{Fe}=\dfrac{11}{3240}\cdot94=\dfrac{517}{1620}\left(mol\right)\)
\(V_{H_2}=7.15\left(l\right)\)

`2Fe + 6H_2 SO_[4(đ,n)] -> Fe_2(SO_4)_3 + 3SO_2 \uparrow + 6H_2 O`
`0,05` `0,15` `0,025` `(mol)`
`Cu + 2H_2 SO_[4(đ,n)] -> CuSO_4 + SO_2 \uparrow + 2H_2 O`
`0,225` `0,45` `0,225` `(mol)`
`n_[SO_2]=[6,72]/[22,4]=0,3(mol)`
Gọi `n_[Fe]=x` ; `n_[Cu]=y`
`=>` $\begin{cases} \dfrac{3}{2}x+y=0,3\\56x+64y=17,2 \end{cases}$
`<=>` $\begin{cases}x=0,05\\y=0,225 \end{cases}$
`@m_[Fe_2(SO_4)_3]=0,025.400=10(g)`
`@m_[CuSO_4]=0,225.160=36(g)`
`@m_[dd H_2 SO_4]=[(0,15+0,45).98]/80 .100=73,5(g)`
Sửa đề: 80% ---> 98% (80% chưa đặc nên không giải phóng SO2 được)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(\rightarrow56a+64b=17,2\left(1\right)\)
PTHH:
\(2Fe+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
a------>3a------------------->0,5a--------------->1,5a
\(Cu+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\)
b----->2b------------------->b------------->b
\(\rightarrow1,5a+b=\dfrac{6,72}{22,4}=0,3\left(2\right)\)
Từ \(\left(1\right)\left(2\right)\rightarrow\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,225\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe_2\left(SO_4\right)_3}=0,5.0,05.400=10\left(g\right)\\m_{CuSO_4}=0,225.160=36\left(g\right)\\m_{ddH_2SO_4}=\dfrac{\left(0,05.3+0,225.2\right).98}{98\%}=60\left(g\right)\end{matrix}\right.\)

Bạn xem hỗn hợp ban đầu được tạo thành từ: Fe, Cu và O2
Fe -------> Fe3+ + 3e
x.........................3x
Cu -------> Cu2+ + 2e
y..........................2y
O2 + 4e -----> 2O2-
z.........4z
S+6 + 2e -------> S+4
...........0,045..........0,0225
Gọi x, y, z là số mol Fe, Cu, O2. Ta có hpt:
56x + 64y + 32z = 2,44
3x + 2y = 4z + 0,045
0,5*400x + 160y = 6,6
=> x = 0,025, y = 0,01, z = 0,0125
=> %mCu = 0,01*64/2,44*100% = 26,23%

Đáp án A.
Gọi nAl = a mol, nZn = b mol.

Ta có: 27a + 65b = 9,2 (*)
3a + 2b = 0,5 (**)
Giải (*), (**): a = b = 0,1 mol.
m muối = mKl + M gốc axit. ne/2
= 3,92 + 96. 0,25 = 33,2 g
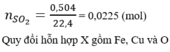
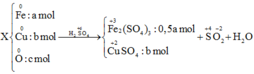
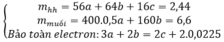
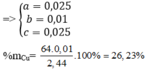





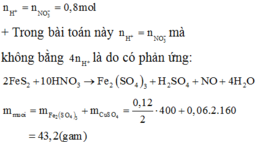


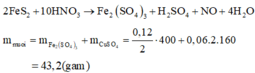
a. Gọi \(a,b\) lần lượt là số mol của \(Mg,Fe\) có trong hỗn hợp ban đầu.
\(\Rightarrow m_{hh}=24a+56b=22,8\left(g\right)\left(1\right)\)
\(n_{SO_2}=\frac{15,68}{22,4}=0,7\left(mol\right)\)
Các quá trình oxi hóa và khử:
\(Mg\rightarrow Mg^{2+}+2e\)
\(a----->2a\)
\(Fe\rightarrow Fe^{3+}+3e\)
\(b----->3b\)
\(S^{+6}+2e\rightarrow S^{+4}\)
\(0,7-1,4-0,7\)
Áp dung định luật bào toàn electron, ta có: \(2a+3b=1,4\left(mol\right)\left(2\right)\)
Từ \(\left(1\right),\left(2\right)\) ta được hệ: \(\left\{{}\begin{matrix}24a+56b=22,8\\2a+3b=1,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,25\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=0,25.24=6\left(g\right)\Rightarrow\%m_{Mg}=\frac{6}{22,8}=.100\%=26,32\%\)
\(\Rightarrow\%m_{Fe}=100\%-26,32\%=73,68\%\)
b. Từ câu a, ta được: \(n_{H_2SO_4\left(p.ư\right)}=n_{S^{+6}}=0,7\left(mol\right)\)
\(n_{NaOH}=0,4.3=1,2\left(mol\right)\)
PTHH: \(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=\frac{1,2}{2}=0,6\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(bđ\right)}=0,7+0,6=1,3\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4\left(bđ\right)}=1,3.98=127,4\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4\left(bđ\right)}=\frac{127,4.100}{98}=130\left(g\right)\)
c. Gọi \(x\) là số mol của \(Cu_2S\) \(\rightarrow n_{FeS_2}=2x\left(mol\right)\)
PTHH:
\(2FeS_2+14H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+14H_2O+15SO_2\)
\(2x---->14x-->x\)
\(Cu_2S+6H_2SO_4\rightarrow2CuSO_4+5SO_2+6H_2O\)
\(x---->6x-->2x\)
\(\Rightarrow14x+6x=1,3\left(mol\right)\Leftrightarrow x=0,065\left(mol\right)\)
\(\Rightarrow n_{Fe_2\left(SO_4\right)_3}=x=0,065\left(mol\right);n_{CuSO_4}=2x=0,13\left(mol\right)\)
\(\Rightarrow m_{Fe_2\left(SO_4\right)_3}=0,065.400=26\left(g\right);m_{CuSO_4}=0,13.160=20,8\left(g\right)\)
\(\Rightarrow m\)muối\(=26+20,8=46,8\left(g\right)\)