Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(\left[H^+\right]=0,01.2=0,02M\)
=> pH = 1,7
b) \(\left[OH^-\right]=0,03.2=0,06M\)
=> pOH= 1,22
=> \(pH=14-1,22=12,78\)
a) pH= -log[H+]= -log[0,01.2]=1,69
b) pH= 14 - pOH= 14 + log[OH-]= 14+ log[0,03.2]=12,78

Đáp án D
nH2SO4 = 0,005 .0,25 =0,00125(mol)
nHCl = 0,01. 0,25= 0,0025 (mol)
∑n= 0,00125 + 0,0025= 0,00375 (mol)
∑n= 0,001.0,2 + 0,0005.2.0,2=0,0004
H+ + OH- → H2O
Ban đầu: 0,00375 0,0004
Phản ứng: 0,0004 0,0004
Sau phản ứng: 0,00335 0
Vsau = 0,2 + 0,25= 0,45(lít)
Mà 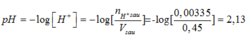

a) pH= -log[H+]= -log[0,1]=1
b) pH= 14- p[OH-]= 14+log[0,1]=13
Bạn ơi bạn có thể cho mình hỏi là pH=14-p(OH-) mà số 14 đó ở đâu ra được hem

$n_{NaOH} = 0,001(mol)$
$n_{Ba(OH)_2} = 0,01.0,15 = 0,0015(mol)$
$NaOH \to Na^+ + OH^-$
$Ba(OH)_2 \to Ba^{2+} + 2OH^-$
Ta có :
$n_{OH^-}= 0,001 + 0,0015.2 = 0,004(mol)$
$V_{dd} = 0,1 + 0,15 = 0,25(mol)$
$[OH^-] = \dfrac{0,004}{0,25} = 0,016M$
$pOH = -log(0,016) = 1,795 \Rightarrow pH = 14 - 1,795 = 12,205$
