Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
a) \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
b) \(Al_2O_3+3H_2\underrightarrow{t^o}2Al+3H_2O\)
c) \(2Zn+O_2\underrightarrow{t^o}2ZnO\)
Câu 2:
\(n_{Fe_2O_3}=\frac{16}{160}=0,1\left(mol\right)\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
0,1_______0,3___0,2_____0,3(mol)
\(m_{Fe}=0,2.56=11,2\left(g\right)\)
Câu 3:
nH2=6,72/22,4=0,3mol
nCuO=8/80=1mol
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
1----------------------------->(mol)
So sánh \(\frac{0,3}{1}>\frac{0,1}{1}\)
a) Chất rắn màu đen chuyển dang màu đỏ và có hơi nước
b) \(m_{Cu}=0,1.64=6,4\left(g\right)\)

Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{CuO}=\dfrac{32}{80}=0,4\left(mol\right)\)
PT: \(H_2+CuO\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,3}{1}< \dfrac{0,4}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,3.64=19,2\left(g\right)\)
→ Đáp án: C
Bạn tham khảo nhé!
Dẫn 6,72 lít khí hiđro đi qua 32 gam đồng (II) oxit nung nóng, phản ứng xảy ra hoàn toàn. Khối lượng đồng thu được là
A.25,6 (g).
B.6,4 (g).
C.19,2(g).
D.24 (g).
\(n_{H_2}=0,3\left(mol\right);n_{CuO}=0,4\left(mol\right)\)
\(H_2+CuO-^{t^o}\rightarrow Cu+H_2O\)
Lập tỉ lệ : \(\dfrac{0,3}{1}< \dfrac{0,4}{1}\Rightarrow\) CuO dư sau pứ
\(n_{Cu}=n_{H_2}=0,3\left(mol\right)\Rightarrow m_{Cu}=0,3.64=19,2\left(g\right)\)
=> Chọn C

\(n_{Cu}=\dfrac{12.8}{64}=0.2\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{t^0}}Cu+H_2O\)
\(0.2......0.2.....0.2\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(m_{CuO}=0.2\cdot80=16\left(g\right)\)

\(n_{Fe_2O_3=}=\dfrac{24}{160}=0,15mol\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,15 0,45 0,3 0,45
\(V_{H_2}=0,45\cdot224,=10,08l\)
\(m_{Fe}=0,3\cdot56=16,8g\)

a. Công thức về khối lượng:
\(m_{Fe_2O_3}+m_{H_2}=m_{Fe}+m_{H_2O}\)
b. Áp dụng câu a, ta có:
\(m_{Fe_2O_3}+2=56+18\)
\(\Leftrightarrow m_{Fe_2O_3}=56+18-2\)
\(\Leftrightarrow m_{Fe_2O_3}=72\left(g\right)\)
\(a)3H_2+Fe_2O_3-^{t^o}\rightarrow2Fe+3H_2O\\b)BTKL:m_{H_2}+m_{Fe_2O_3}=m_{Fe}+m_{H_2O}\\ \Leftrightarrow2+m_{Fe_2O_3}=56+18 \\ \Rightarrow m_{Fe_2O_3}=72\left(g\right)\)

\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ pthh:Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2 0,4 0,2
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\\ V_{H_2}=0,2.22,4=4,48\left(l\right)\\ pthh:FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
0,2 0,2 0,2
\(m_{Fe}=0,2.56=11,2\left(g\right)\)

Ta có: \(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
\(PTHH:\)
\(Fe+2HCl--->FeCl_2+H_2\left(1\right)\)
\(CuO+H_2\overset{t^o}{--->}Cu+H_2O\left(2\right)\)
a. Theo PT(1): \(n_{H_2}=n_{Fe}=0,15\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,15.22,4=3,36\left(lít\right)\)
b. Ta thấy: \(\dfrac{0,15}{1}< \dfrac{0,2}{1}\)
Vậy CuO dư.
Theo PT(2): \(n_{Cu}=n_{H_2}=0,15\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)\)

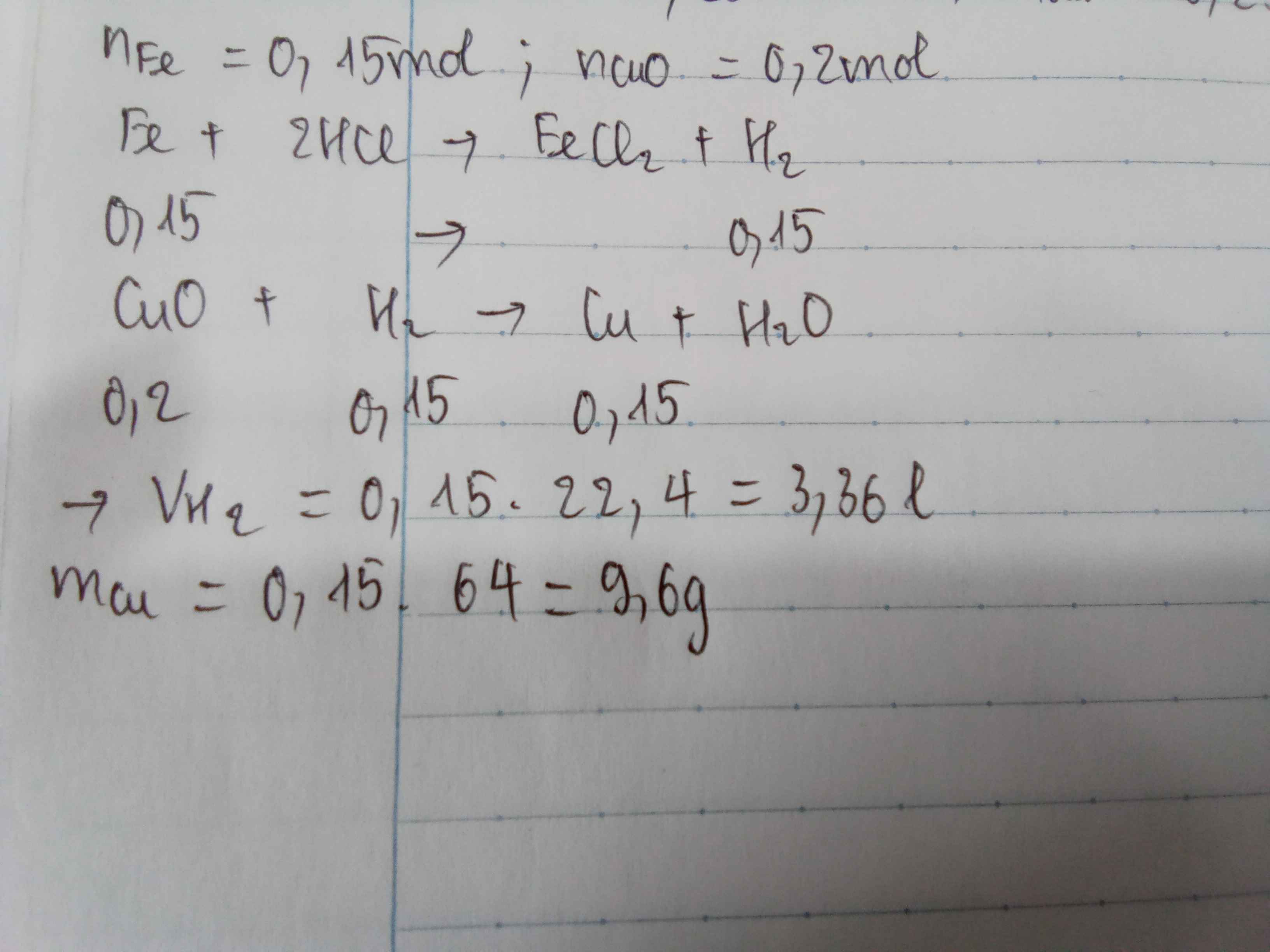


Câu 1:
PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Ta có: \(n_{Fe_2O_3}=\dfrac{16}{160}=0,1 \left(mol\right)\)
\(\Rightarrow n_{Fe}=0,2\left(mol\right)\) \(\Rightarrow m_{Fe}=0,2\cdot56=11,2\left(g\right)\)
Câu 2:
PTHH: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
a) Hiện tượng: Xuất hiện chất rắn màu đỏ và có hơi nước
b) Ta có: \(\left\{{}\begin{matrix}n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,1}{1}\) \(\Rightarrow\) H2 còn dư, CuO p/ứ hết
\(\Rightarrow n_{Cu}=0,1\left(mol\right)\) \(\Rightarrow m_{Cu}=6,4\left(g\right)\)