
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Bài 8:
a). 2NaOH + H2SO4 → Na2SO4 + 2H2O
2 1 1 2
0,6 0,3 0,3 0,6
200ml = 0,2l
nH2SO4= CM . V = 1,5 . 0,2 = 0,3 (mol)
nNaOH = \(\dfrac{0,3.2}{1}\)= 0,6(mol)
mNaOH= n . M = 0,6 . 40 = 24(g)
⇒ mddNaOH = \(\dfrac{m_{ct}.100\%}{C\%}\)= \(\dfrac{24.100\%}{20\%}\)= 120(g).
b). Ta có: mH2SO4= n . M = 0,3 . 98 =29,4(g).
mH2O = n . M = 0,6 . 18 = 10,8 (g).
Ta lại có: mddNa2SO4 = mddNaOH + mH2SO4 - mH2O
= 120 + 29,4 - 10,8
= 138,6(g).
mctNa2SO4= n . M = 0,3 . 142 = 42,6(g)
C%Na2SO4 = \(\dfrac{m_{ct}}{m_{dd}}\).100%=\(\dfrac{42,6}{138,6}\).100% ∼ 30,74%
Bài 9:
Đặt công thức oxit của KL là RO
RO + 2HCl → RCl2 + H2O
Ta có: mHCl =\(\dfrac{600.3,65}{100\%}\)= 21,9(g)
⇒nHCl = \(\dfrac{21,9}{36,5}\)= 0,6(mol).
Từ PT trên, có: nRO = \(\dfrac{1}{2}\)nHCl =0,3(mol)
2,4 : (R+16) =0,3
tự bấm ra kq nhé, bị bắt đi ngủ r:) thông cảm ạ


6
Gọi x , y lần lượt là số mol của Al và Fe
\(n_{H_2}\)\(=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2 \)
x \(\rightarrow\) \(\dfrac{3}{2}x\) (mol)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
y \(\rightarrow\) y (mol)
Từ trên ta có hpt
\(\left\{{}\begin{matrix}27x+56y=11\\\dfrac{3}{2}x+y=0.4\end{matrix}\right.\)
giải ra ta được
x=0.2-) mAl=0.2*27=5.4(g) =))\(\%Al=\dfrac{5.4}{11}\cdot100=49.1\%\)
y=0.1-)mFe=0.1*56=5.6(g) =))\(\%Fe=\dfrac{5.6}{11}\cdot100=50.9\%\)
5
Cu không pư được H2SO4 nên 6.4(g) chất rắn còn lại sau pư là Cu
\(m_{Fe}=10-6.4=3.6\left(g\right)\)
pthh:
\(Fe+H_2So_4\Rightarrow FeSo_4+H_2\)
\(\left\{{}\begin{matrix}\%Cu=\dfrac{0.1\cdot64}{10}\cdot100=64\%\\^{\%Fe=\dfrac{3.6}{10}\cdot100=36\%}\end{matrix}\right.\)


\(a) Mg + 2CH_3COOH \to (CH_3COO)_2Mg + H_2\\ n_{H_2} = n_{Mg} = \dfrac{9,6}{24} = 0,4(mol)\\ V_{H_2} = 0,4.22,4 = 8,96(lít)\\ b) n_{(CH_3COO)_2Mg} = n_{Mg} = 0,4(mol)\\ m_{Muối} = 0,4.142 = 56,8(gam)\\ c) n_{CH_3COOH} = 2n_{Mg} = 0,8(mol)\\ m_{dd\ CH_3COOH} = \dfrac{0,8.60}{6\%} = 800(gam)\\ d) C_2H_5OH + O_2 \xrightarrow{men\ giấm} CH_3COOH + H_2O\\ n_{C_2H_5OH} = n_{CH_3COOH} = 0,8(mol)\\ m_{C_2H_5OH} = 0,8.46 = 36,8(gam)\)

Mình đang càn gấp câu c ạ, mọi người giúp mình câu c được không ạ??
Gọi nMg=x mol, nAl=y mol
nH2=\(\dfrac{5,6}{22,4}=0,25mol\)
Mg + 2HCl → MgCl2 + H2
x → 2x → x → x
2Al + 6HCl → 2AlCl3 + 3H2
y → 3y → y → 1,5y
\(\left\{{}\begin{matrix}24x+27y=5,1\\x+1,5y=0,25\end{matrix}\right.\) ⇔ \(\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
a) %Mg=\(\dfrac{0,1.24}{5,1}.100\%\approx47,06\%\)
%Al = 100% - 47,06%=52,94%
b) nHCl=2x+3y=0,1.2+0,1.3=0,5 mol
mHCl = 0,5 . 36,5=18,25g
m=\(\dfrac{18,25.100}{10}=182,5g\)
c) MgCl2 + 2NaOH → Mg(OH)2 + 2NaCl
x → x
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
y → y
a = mMg(OH)2 + mAl(OH)3
= 0,1.58 + 0,1.78 =13,6g

5.
\(n_{Na}=a\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(a...............a.....0.5a\)
\(m_{\text{dung dịch sau phản ứng}}=23a+500-0.5a\cdot2=22a+500\left(g\right)\)
\(m_{NaOH}=40a\left(g\right)\)
\(C\%_{NaOH}=\dfrac{40a}{22a+500}\cdot100\%=20\%\)
\(\Rightarrow a=2.8\)
\(b.\)
\(n_{H^+}=10^{-3}\cdot V\cdot\left(1+0.5\cdot2\right)=2\cdot10^{-3}V\left(mol\right)\)
\(\Rightarrow n_{NaOH}=2\cdot10^{-3}V=2.8\left(mol\right)\)
\(\Rightarrow V=1400\)

Bài 2 :
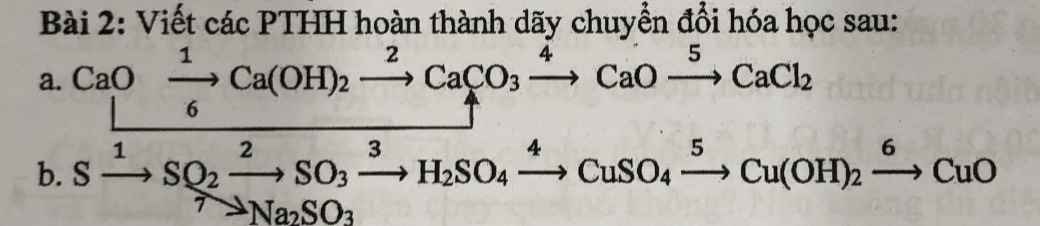
a) (1) \(CaO+CO_2\rightarrow CaCO_3\)
(2) \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
(3) \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
(4) \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
(5) \(CaO+2HCl\rightarrow CaCl_2+H_2O\)
Chúc bạn học tốt
b)(1) \(S+O_2\underrightarrow{t^o}SO_2\)
(2) \(2SO_2+O_2\underrightarrow{t^o,V_2O_5}2SO_3\)
(3) \(SO_3+H_2O\rightarrow H_2SO_4\)
(4) \(H_2SO_4+CuO\rightarrow CuSO_4+H_2O\)
(5) \(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
(6) \(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
(7) \(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
Chúc bạn học tốt




 mọi người giúp em với em cần gấp <3
mọi người giúp em với em cần gấp <3

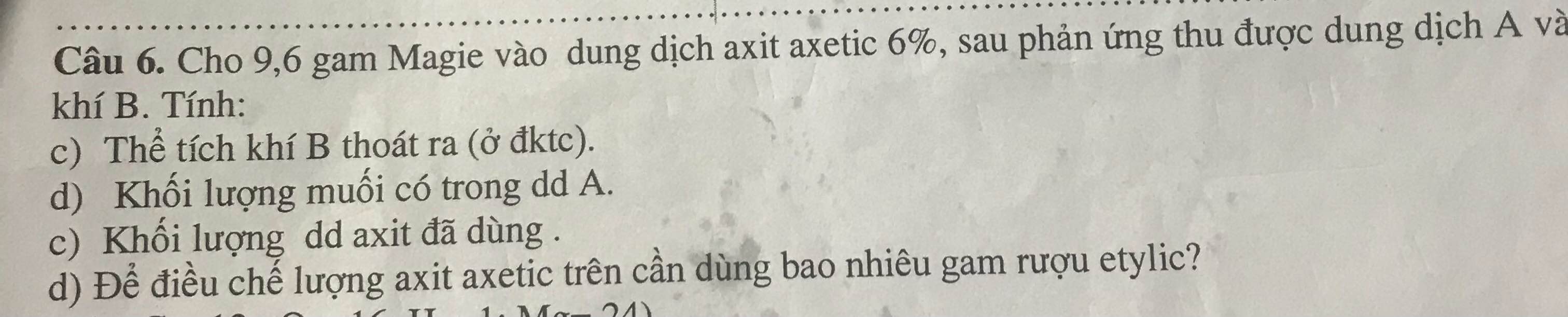


Bài 1:
PTHH: \(K_2CO_3+2HCl\rightarrow2KCl+CO_2\uparrow+H_2O\)
a_____2a______2a______a (mol)
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2\uparrow+H_2O\)
b_____2b_______2b______b (mol)
a) Ta lập HPT: \(\left\{{}\begin{matrix}138a+106b=4,72\\a+b=\dfrac{0,896}{22,4}=0,04\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,015\\b=0,025\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{K_2CO_3}=\dfrac{138\cdot0,015}{4,72}\cdot100\%\approx43,86\%\\\%m_{Na_2CO_3}=56,14\%\end{matrix}\right.\)
b+c) Theo các PTHH: \(\left\{{}\begin{matrix}n_{NaCl}=0,05\left(mol\right)\\n_{KCl}=0,03\left(mol\right)\\n_{HCl}=0,08\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{muối}=0,05\cdot58,5+0,03\cdot74,5=5,16\left(g\right)\\C_{M_{HCl}}=\dfrac{0,08}{0,1}=0,8\left(M\right)\end{matrix}\right.\)
Bài 2:
Ta có: \(\left\{{}\begin{matrix}n_{Mg}=\dfrac{0,6}{24}=0,025\left(mol\right)\\n_{H_2\left(axit\:\right)}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\end{matrix}\right.\)
PTHH: \(Al+NaOH+H_2O\rightarrow NaAlO_2+\dfrac{3}{2}H_2\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
0,025____________________0,025 (mol)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\)
0,03_______________________0,045 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,6}{0,6+0,03\cdot27}\cdot100\%\approx42,55\%\\\%m_{Al}=57,45\%\end{matrix}\right.\)