Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Ca\left(OH\right)_2}=\dfrac{7,4}{74}=0,1\left(mol\right)\)
PTHH: CaO + H2O --> Ca(OH)2
0,1<--------------0,1
=> mCaO = 0,1.56 = 5,6 (g)



Trong phòng thí nghiệm, người ta điều chế khí oxi bằng cách nhiệt phân KClO₃ hay KMnO₄ vì giàu oxi và dễ phân hủy tạo ra oxi

$a)2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$b) n_{KClO_3} = \dfrac{73,5}{122,5} = 0,6(mol)$
$n_{KCl} = n_{KClO_3} = 0,6(mol)$
$m_{KCl} = 0,6.74,5 = 44,7(gam)$
$c) n_{O_2} = \dfrac{3}{2}n_{KClO_3} = 0,9(mol)$
$V_{O_2} = 0,9.22,4 = 20,16(lít)$

1) nFe3O4= 46,4:232=0,2 mol
PTHH :3Fe+2O2\(\rightarrow\) Fe3O4
0,6 0,4 \(\leftarrow\)0,2 (mol)
PTHH: 2KMnO4\(\rightarrow\) K2MnO4+MnO2+O2
0,8 \(\leftarrow\) 0,4 (mol)
\(\Rightarrow\) m KMnO4= 0,8.158=126,4 g
1) 3Fe + 2O2 ---> Fe3O4 ---> nO2 = 2nFe3O4 = 2.46,4/232 = 0,4 mol.
2KMnO4 ---> K2MnO4 + MnO2 + O2 ---> nKMnO4 = 2nO2 = 0,8 mol
---> mKMnO4 = 158.0,8 = 126,4 g.
2) KClO3 ---> KCl + 3/2O2 ---> nKClO3 = 2/3nO2
---> nKClO3:nKMnO4 = 2/3:2 = 1:3 ---> mKClO3:mKMnO4 = 158/3.122,5 = 0,43
3) KNO3 ---> KNO2 + 1/2O2 ; Cu(NO3)2 ---> CuO + 2NO2 + 1/2O2
Như vậy nếu thu được cùng lượng oxi thì KClO3 sẽ có khối lượng nhỏ nhất.

1.
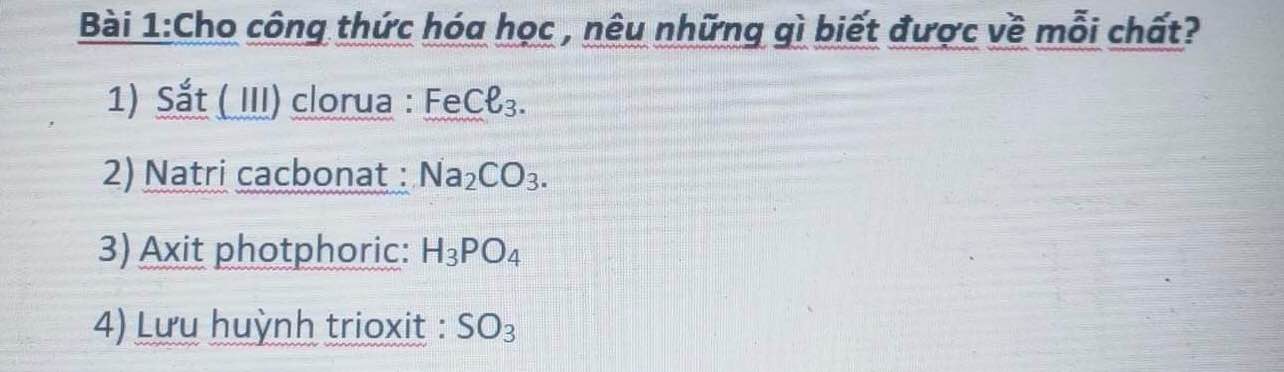
- Hợp chất cấu tạo từ 2 nguyên tố: Fe và Cl
- Hợp chất có: 1 nguyên tố Fe và 3 nguyên tố Cl
- PTK=56+35,5 x 3=162,5(đvC)PTK=56+35,5 x 3=162,5(đvC)
===========
2.
- Hợp chất cấu tạo từ 3 nguyên tố: Na, C và O
- Hợp chất có: 2 nguyên tố Na, 1 nguyên tố C và 3 nguyên tố O
- PTK=23 x 2+12+16 x 3=106(đvC)PTK=23 x 2+12+16 x 3=106(đvC)
==========
3.
- Hợp chất cấu tạo từ 3 nguyên tố: H, P và O
- Hợp chất có: 2 nguyên tố H, 1 nguyên tố P và 4 nguyên tố O
- PTK=1 x 3+31+16 x 4=98(đvC)PTK=1 x 3+31+16 x 4=98(đvC)
==========
4.
- Hợp chất cấu tạo từ 2 nguyên tố: S và O
- Hợp chất có: 1 nguyên tố S và 3 nguyên tố O
- PTK=32+16 x 3=80(đvC)


-Thí nghiệm: Cho một ít KMnO4 hoặc KClO3 vào ống nghiệm có cắm ống dẫn khí,đầu ống nghiệm được nút lại.
Câu hỏi là: cách điều chế oxi trong phòng thí nghiệm á
Giúp mình đi mọi ngừi ơiii 😥🥺