Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. PTK của hợp chất nặng hơn phân tử hidro 31 lần
Phân tử khối của phân tử hidro là 1.2 = 2 đvC
⇒ Phân tử khối của hợp chất là: 2.31 = 62 đvC
b. PTK hợp chất = 2.NTK X + 1.NTK O = 62 đvC
⇒ 2.NTK X + 16 = 62 đvC
Vậy nguyên tử khối của X là 23. Nguyên tố X là natri (Na)
bỏ chữ
b. PTK hợp chất = 2.NTK X + 1.NTK O = 62 đvC
⇒ 2.NTK X + 16 = 62 đvC
bạn viết là 2X+1O = 62 đvC cũng đủ hiểu mà ![]()

4674449991663564477889332677886433235689988766554332134566789[00987766555443221234455667789008766543213¹12345678997775764665765576675675775554889888888884444444499999997655777777777777777777⁷77777777777542453353456799987677677677775544655455455565565544666777874332245666666tggf66ggg66hgg
Fhugj
Ggghhhgg
Jkjjn
Tyigv
Rơôâgagu
Jfggtg
Tjhgug
666

\(PTK_{hc}=2.NTK_R+5.NTK_O\\ \Leftrightarrow71.2=NTK_R+5.16\\ \Leftrightarrow NTK_R=31\left(đ.v.C\right)\\ \Rightarrow R:Photpho\left(NTK_P=31\left(đ.v.C\right)\right)\\ \)

Ta có :
PTKCa = 40 (đvC)
=> PTKhợp chất A = 40(đvC)
Do trong hợp chất A có chứa 60% Mg(1)
=> Khối lượng của Mg trong hợp chất A là :
40 * 60% = 24 (đvC)
Mà NTKMg = 24 đvC => có 1 nguyên tử Mg trong hợp chất A(*)
Tù (1) => % của Oxi trong hợp chất A là :
100% - 60% = 40%
=> Khối lượng của Oxi trong hợp chất A là :
40 * 40% = 16 (đvC)
Mà NTKO = 16 đvC => có 1 nguyên tử O trong hợp chất A (**)
Từ (*) và (**) => công thức hóa học của hợp chất A là :
CuO
%mO = 100%-60%=40%
Công thức chung của h/c : MgxOy
Ta có : x : y = \(\frac{60\%}{24}:\frac{40\%}{16}\)=2,5 : 2,5 = 1 : 1
=> CTHH h/c A : MgO
Ta có : MA=MCa=40 g/mol
Mà MMgO= 24 + 16 = 40
=> CTHH : MgO
( Mấy bài dạng này làm lâu rồi nên mình cũng quên cách làm mất không biết đúng không bạn cứ tham khảo )
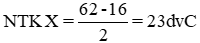

biết \(M_O=16\left(đvC\right)\)
\(\Rightarrow\)\(M_X=2,5.16=40\left(đvC\right)\)
\(\Rightarrow X\) là \(Ca\)