Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

mdd giảm = m↓ - mCO2 → mCO2 = 10 - 3,4 = 6,6 gam → nCO2 = 6,6 : 44 = 0,15 mol.
C6H12O6 enzim−−−−→30−35oC→30-35oCenzim2C2H5OH + 2CO2
Theo phương trình: nC6H12O6 = 0,15 : 2 = 0,075 mol.
Mà H = 90% → nC6H12O6 = 0,075 : 90% = 1/12 mol → m = 180 x 1/12 = 15 gam

a) Các phương trình phản ứng:
C2H4 + Br2 → C2H4Br2
C2H2 + 2Br2 → C2H2Br4
C2H2 + Ag2O → C2Ag2 + H2O
Hay
C2H2 + 2AgNO3 + 2NH3 → C2Ag2 + 2NH4NO3
b) Gọi a, b, c lần lượt là số mol của CH4, C2H4, C2H2 trong 4,3gam hỗn hợp T.
– Số mol Br2 = 0,15 (mol); số mol kết tủa = số mol C2H2 = 0,075 (mol); số mol T = 0,3 (mol). Do đó nT = 4nC2H2
– Ta có hệ phương trình:
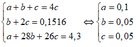
– Suy ra % thể tích mỗi khí trong T:
%VCH4 = 50%; %VC2H2 = %VC2H4 = 25%

- Phần 1 tác dụng với Br2: nBr2 = 16:160 = 0,1 mol
C2H2 + 2Br2 → C2H2Br4
0,05 ← 0,1 (mol)
- Đặt số mol khí mỗi phần như sau:
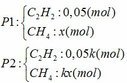
+ Số mol hỗn hợp khí X là: nX = 11,2:22,4 = 0,5 mol
Ta có: n khí P1 + n khí P2 = nX => 0,05 + x + 0,05k + kx = 0,5 <=> (x + 0,05)k = 0,45 - x
=> 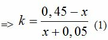
+ Đốt cháy phần 2:
C2H2 + 2,5O2 → t ∘ 2CO2 + H2O
0,05k → 0,1k→ 0,05k (mol)
CH4 + 2O2 → t ∘ CO2 + 2H2O
kx → kx → 2kx (mol)
Sản phẩm cháy gồm
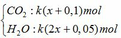
dẫn qua dung dịch Ba(OH)2 dư:
CO2 + Ba(OH)2 → BaCO3↓ + H2O
k(x+0,1) → k(x+0,1) (mol)
Khối lượng dung dịch giảm: m dd giảm = mBaCO3 – mCO2 – mH2O
=> 197k(x+0,1) – 44k(x+0,1) – 18k(2x+0,05) = 69,525
=> 153k(x+0,1) – 18k(2x+0,05) = 69,525
=> k(117x+14,4) = 69,525
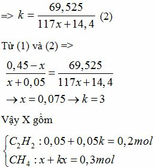
CaC2 + 2H2O → Ca(OH)2 + C2H2
0,2 ← 0,2 (mol)
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4
0,1 ← 0,1 (mol)
Giá trị của m là: m = mCaC2 + mAl4C3 = 0,2.64 + 0,1.144 = 27,2 gam
Phần trăm thể tích các khí trong X là:

tác dụng với AgNO3 trong NH3 dư:
C2H2 + 2AgNO3 + 2NH3 → Ag2C2↓ + 2NH4NO3
0,15 → 0,15 (mol)
Khối lượng kết tủa thu được là: mAg2C2 = 0,15.240 = 36 gam

nH2 = 0,13 mol; nSO2 = 0,25 mol
Ta có
2H+ + 2e → H2 Cu → Cu2+ + 2e
0,26 ←0,13 0,12 0,24
S+6 + 2e → S+4
0,5 ← 0,25
TH1: M là kim loại có hóa trị không đổi
=> nCu = (0,5 – 0,26) : 2 = 0,12 mol => mCu = 7,68g
=> mM = 3,12g (loại vì khối lượng của M lớn hơn của Cu)
TH2: M là kim loại có hóa trị thay đổi
Do M không có hóa trị I do đó khi phản ứng với HCl thì M thể hiện hóa trị II
M + 2HCl → MCl2 + H2
0,13 ← 0,13
Do M có hóa trị thay đổi => khi phản ứng với H2SO4 đặc nóng thì M thể hiện hóa trị III
2M + 6H2SO4 → M2(SO4)3 + 3SO2 + 6H2O
0,13 → 0,195
Cu + 2H2SO4 → CuSO4+ SO2 + 2H2O
0,055 ← 0,055
=> mM = 10,8 – 0,055 . 64 = 7,28g
=> MM = 56 => Fe
Ta có số mol của Cu và Fe trong 10,8 g lần lượt là 0,055 và 0,13 mol
=> Trong 5,4g có số mol Cu và Fe lần lượt là 0,0275 và 0,065 mol
nAgNO3 = 0,16mol
Fe + 2AgNO3 → Fe(NO3)2 +2Ag
0,065 0,13 0,065 0,13
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
0,015 0,03 0,03
=> nCu dư = 0,0275 – 0,015 = 0,0125mol
m = mCu dư + mAg = 0,0125 . 64 + 0,16 . 108 = 18,08g

a.

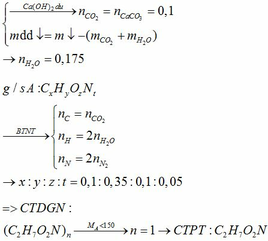
b.
Vì A pứ với NaOH nên CTCT của A là: CH3COONH4 hoặc HCOONH3CH3
Y pứ ở 15000C nên Y là: CH4
=> X: CH3COONa → A:CH3COONH4
Z: CH≡CH → T: CH3CHO
Vậy A là: CH3COONH4 (amoniaxetat)

\(V_{C_2H_6}=13,44-6,72=6,72\left(l\right)\)
=> \(n_{C_2H_6}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{C_2Ag_2}=\dfrac{24}{240}=0,1\left(mol\right)\)
=> \(n_{C_2H_2}=0,1\left(mol\right)\)
=> \(n_{C_2H_4}=\dfrac{13,44}{22,4}-0,3-0,1=0,2\left(mol\right)\)
=> \(\left\{{}\begin{matrix}\%m_{C_2H_6}=\dfrac{0,3.30}{0,3.30+0,2.28+0,1.26}.100\%=52,326\%\\\%m_{C_2H_4}=\dfrac{0,2.28}{0,3.30+0,2.28+0,1.26}.100\%=32,558\%\\\%m_{C_2H_2}=\dfrac{0,1.26}{0,3.30+0,2.28+0,1.26}.100\%=15,116\%\end{matrix}\right.\)


=> nX+T = 0,12
=> nCO2 – nH2O = 0,5 – 0,36 = 0,14 >nT
=> Y là axit không no
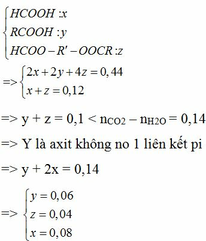
nCO2 = 1 . 0,08 + b . 0,06 + c . 0,04 = 0,5 (với b là số nguyên tử C trong Y và c là số nguyên tử C trong T)
1,5b + c = 10,5
=> 3b +2c = 21
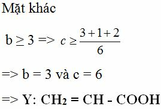
T: CH2 = CH – COO – CH2 – CH2 - OOCH



TN2: C3H4 + AgNO3 + NH3 = C3H3Ag + NH4NO3
nC3H3Ag= 0.15 mol Từ PTHH: nC3H4= 0.15 mol mC3H4= 6g TN1: nCO2= 0.85 mol C3H4 + 4O2 -to-> 3CO2 + 2H2O 0.15____________0.45 C2H4 + 3O2 -to-> 2CO2 + 2H2O 0.2_____________0.85-0.45 mC2H4= 5.6g %C3H4= 6/(6+5.6)*100%= 51.72% %C2H2= 48.28%