Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nS=mS/MS=3,2/32=0,1(mol)
nO2=VO2/22,4=32/22,4=1,42(mol)
PTHH: S + O2 --> SO2 (1)
BĐ: 0,1 1,42
PỨ: 0,1-->0,1-->0,1
SPỨ: 0--->1,32-->0,1
a) Từ PT(1)=>O2 dư
VO2(dư)=nO2(dư) .22,4=1,32 .22,4=29,568(l)
b) Từ PT(1)=>nSO2=0,1(mol)
=>mSO2=n.M=0,1 .64=6,4(g)
Mình sửa lại nha mình nhầm ạ

Bài 1:
a) PTHH: C+ O2 -to-> CO2
Theo PTHH và đề bài, ta có:
\(n_{O_2}=n_C=5\left(mol\right)\)
Khối lượng khí O2 cần dùng cho phản ứng:
\(m_{O_2}=n_{O_2}.M_{O_2}=5.32=160\left(g\right)\)
Bài 1 mình không hiểu lắm.
Mình làm bài 2 nha.
Bài 2:
Ta có:
\(n_S=\frac{m_S}{M_S}=\frac{3,2}{32}=0,1\left(mol\right)\)
\(n_{O_2}=\frac{V_{O_2}}{22,4}=\frac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: S + O2 -to-> SO2
Theo PTHH và đề bài ta có:
\(\frac{n_{S\left(đềbài\right)}}{n_{S\left(PTHH\right)}}=\frac{0,1}{1}=0,1>\frac{n_{O_2\left(đềbài\right)}}{n_{O_2\left(PTHH\right)}}=\frac{0,05}{1}=0,05\)
Vậy: O2 phản ứng hết còn S dư .

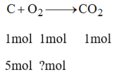
Số mol O 2 :
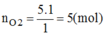
Khối lượng O 2 :
m O 2 = n O 2 . M O 2 = 5.32 = 160(g)
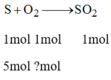
Số mol O 2 :
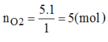
Khối lượng O 2 :
m O 2 = n O 2 . M O 2 = 5.32 = 160(g)

\(n_S=\dfrac{6,4}{32}=0,2mol\)
\(n_{O_2}=\dfrac{16}{32}=0,5mol\)
\(S+O_2\underrightarrow{t^o}SO_2\)
0,2 0,5 0,2
Sau phản ứng oxi còn dư và dư \(0,5-0,2=0,3mol\)
Oxit axit được tạo thành là \(SO_2\) và có khối lượng:
\(m_{SO_2}=0,2\cdot64=12,8g\)

\(n_S=\dfrac{1,6}{32}=0,05\left(mol\right)\)
\(n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
PT: \(S+O_2\underrightarrow{t^o}SO_2\)
Xét tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,1}{1}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=n_S=0,05\left(mol\right)\Rightarrow n_{O_2\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\)
\(\Rightarrow m_{O_2\left(dư\right)}=0,05.32=1,6\left(g\right)\)

a, PTHH: C + O2 ➝ CO2
Theo pt: 1 1 1 (mol)
Theo bài ra: 5 → 5 (mol)
⇒mO2= 5x32= 160(g)
PTHH: S + O2 ➞ SO2
Theo pt: 1 1 1 (mol)
Theo bài ra: 5 → 5 (mol)
⇔mO2= 5x32=160(g)
b, nO2= 1,12/22,4=0,05(mol)→mO2=1,6(g)
PTHH: S + O2 ➝ SO2
Theo pt: 32 32 64 (g)
Theo bài ra: 3,2 1,6 (g)
Phản ứng: dư hết
⇒mS dư = 3,2 - 1,6=1,6(g)
Vậy lưu huỳnh dư và dư 1,6g
TICK CHO MIK NHOA!!!
a, \(C+O_2\underrightarrow{^{to}}CO_2\)
\(n_{O2}=5\left(mol\right)\rightarrow m_2=160\left(g\right)\)
\(S+O_2\underrightarrow{^{to}}SO_2\)
\(n_{O2}=5\left(mol\right)\rightarrow m_{O2}=160\left(g\right)\)
b, \(n_S=0,1\left(mol\right);n_{O2}=0,05\left(mol\right)\)
Nên S dư 0,05 (mol) \(\rightarrow m_{S_{du}}=1,6\left(g\right)\)