Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CaCO3 --to--> CaO + CO2
Theo ĐLBTKL: mCaCO3 (pư) = mCaO + mCO2
=> mCaCO3(pư) = 56 + 44 = 100 (g)
=> \(\%CaCO_3=\dfrac{100}{200}.100\%=50\%\)
=> D

- Cốc A: \(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(n_{CaCO_3}=\dfrac{25}{100}=0,25\left(mol\right)=n_{CO_2}\)
Có: m cốc A tăng = mCaCO3 - mCO2 = 25 - 0,25.44 = 14 (g) = m cốc B tăng
- Cốc B: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
GọI: nAl = x (mol) \(\Rightarrow n_{H_2}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}x\left(mol\right)\)
Có: m cốc B tăng = 14 (g) = 27x - 3/2x.2
⇒ x = 7/15 (mol)
\(\Rightarrow a=m_{Al}=\dfrac{7}{15}.27=12,6\left(g\right)\)

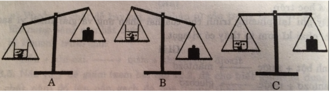
Chọn B. Vì khi cho đá vôi vào dung dịch axit clohiric có phản ứng sinh ra khí cacbon dioxit thoát ra ngoài làm cho khối lượng sẽ giảm đi.

Thí nghiệm 1 : n Na = 1,15/23 = 0,05(mol)
2Na + 2HCl → 2NaCl + H2
Theo PTHH : n H2 = 1/2 n Na = 0,025(mol)
=> m tăng = m Na - m H2 = 1,15 - 0,025.2 = 1,1(gam)
Thí nghiệm 2 :
Mg + H2SO4 → MgSO4 + H2
n H2 = n Mg = a(mol)
=> m tăng = 24a -2a = 22a
Vì hai cân ở vị trí cân bằng <=> 22a = 1,1 <=> a= 0,05
Suy ra : m Mg = 0,05.24 = 1,2(gam)

Giả sử ban đầu mcốc A = mcốc B = m (g)
- Xét cốc A:
\(n_{Na}=\dfrac{1,15}{23}=0,05\left(mol\right)\)
PTHH: 2Na + 2HCl --> 2NaCl + H2
0,05-------------------->0,025
=> mcốc A (sau pư) = m + 1,15 - 0,025.2 = m + 1,1 (g)
- Xét cốc B
Gọi số mol Mg thêm vào là a (mol)
PTHH: Mg + 2HCl --> MgCl2 + H2
a---------------------->a
=> mcốc B (sau pư) = m + 24a - 2a = m + 22a (g)
Do mcốc A (sau pư) = mcốc B (sau pư)
=> m + 1,1 = m + 22a
=> a = 0,05 (mol)
=> mMg = 0,05.24 = 1,2 (g)