Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt \(n_{KClO_3}=c\left(mol\right)\)
\(n_{KCl}=0,2\left(mol\right)\)
\(BTNT.Cr\Rightarrow n_{K_2Cr_2O_7}=\frac{1}{2}n_{CrCl_3}=0,5b\left(mol\right)\\ BTNT.Mn\Rightarrow n_{KMnO_4}=n_{MnCl_2}=a\left(mol\right)\\ \Rightarrow m_X=158x+122,5c+147b=57,45\left(1\right)\\ BTNT.K\Rightarrow n_{KCl}=n_{KMnO_4}+n_{KClO_3}+2n_{K_2Cr_2O_7}\\ =a+b+c=0,4\left(2\right)\\ \text{Mà }2a=b\left(3\right)\)
\(\left(1\right);\left(2\right);\left(3\right)\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\\c=0,1\end{matrix}\right.\)
QT nhường e:
Mn+7 + 5e ----> Mn+2
0,1_____0,5
Cl+5 + 6e ----> Cl-
0,1____0,6
Cr2+6 + 6e ----> 2Cr+3
_______0,6______0,2
QT nhận e: 2Cl- ----> Cl2 + 2e
BT e \(\Rightarrow n_{Cl_2}=0,85\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=19,04\left(l\right)\)
Chọn A
Gọi số mol KMnO4;KClO3;K2Cr2O7 lần lượt là x, y, z.
\(\Leftrightarrow158x+122,5y+294z=57,45\left(1\right)\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
\(K_2Cr_2O_7+14HCl\rightarrow2KCl+2CrCl_3+3Cl_2+7H_2O\)
\(n_{KCl}=\frac{29,8}{74,5}=0,4\left(mol\right)\)
\(\Leftrightarrow x+y=2z=0,4\left(2\right)\)
\(\left\{{}\begin{matrix}n_{MgCl2}:x\left(mol\right)\\n_{CrCl3}:y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\frac{x}{2z}=\frac{1}{2}\Rightarrow x-z=0\left(3\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,1\left(mol\right)\\z=0,1\left(mol\right)\end{matrix}\right.\)
\(\Leftrightarrow n_{Cl2}=2,5x+3y+3z=2,5.0,1+3.0,1+3.0,1=0,85\left(mol\right)\)
\(\Rightarrow V=0,85.22,4=19,04\left(l\right)\)
Vậy đáp án đúng : A

Gọi :
\(n_{KMnO_4} = n_{K_2Cr_2O_7} = n_{K_2MnO_4} = n_{MnO_2} = n_{PbO_2} = x(mol)\)
Suy ra : 975x = m(1)
Bảo toàn nguyên tố với K,Mn,Cr,Pb ,Muối gồm :
\(\left\{{}\begin{matrix}KCl:x+2x+2x=5x\left(mol\right)\\MnCl_2:x+x+x=3x\left(mol\right)\\CrCl_3:2x\left(mol\right)\\PbCl_2:x\left(mol\right)\end{matrix}\right.\)
Suy ra : 1345,5x = m + 11,856(2)
Từ (1)(2) suy ra : m = 31,2 ; x = 0,032
Bảo toàn electron :
\(5n_{KMnO_4} + 6n_{K_2Cr_2O_7} + 4n_{K_2MnO_4} + 2n_{MnO_2} + 2n_{PbO_2} = 2n_{Cl_2}\)
Suy ra :
\(a = \dfrac{0,032.5+0,032.6 + 0,032.4 + 0,032.2 + 0,032.2}{2} = 0,304(mol)\)
(Đáp án B)

\(n_{Cl_2}=\dfrac{2,1168}{22,4}=0,0945\left(mol\right)\)
=> nCl(muối) = 0,39 - 0,0945 = 0,201 (mol)
=> nAgCl = 0,201 (mol)
=> mAgCl = 0,201.143,5 = 28,8435 (g)

Câu 44
Phản ứng điều chế là KClO3 vs HCl
\(n_{KCl}=\frac{17,433}{74,5}=0,234\left(mol\right)\)
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
0,0624_______________0,1872________
\(3Cl_2+6KOH\rightarrow KClO_3+5KCl+3H_2O\)
0,1404__________________0,234__________
\(n_{Cl\left(lt\right)}=\frac{0,1404}{75\%}=0,1872\left(mol\right)\)
\(\Rightarrow m_{KClO3}=0,0624.122,5=7,644\)
Câu 45
\(n_{Cl2}=\frac{17,92}{22,4}=0,8\left(mol\right)\)
Gọi số mol KMnO4;K2Cr2O7 lần lượt là a;ba;b
Phản ứng xảy ra:
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+6H_2O\)
\(14HCl+K_2Cr_2O_7\rightarrow2KCl+2CrCl_3+3Cl_2+7H_2O\)
Ta có hệ phương trình:
\(\left\{{}\begin{matrix}158x+194y=61\\2,4x+3y=0,8\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n\%_{KMnO4}=\frac{0,2}{01+0,2}.100\%=66,67\%\)
\(\Rightarrow\%n_{K2Cr2O7}=100\%-66,67\%=33,33\%\)
Cái hệ của câu 45 mk bấm lại ra âm bn , bn giải thích cho mk vs đc k

- Theo bài ra \(\Rightarrow\left\{{}\begin{matrix}n_{KMnO_4}=0,1\\n_{KClO_3}=0,15\end{matrix}\right.\) ( mol )
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
.......0,1..........................................................0,25...........
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
....0,15................................0,45....................
\(\Rightarrow n_{HCl}=0,7\left(mol\right)\)
\(6KOH+3Cl_2\rightarrow KClO_3+5KCl+3H_2O\)
Ta có : \(m=m_{KOH}+m_{Cl_2}=139,3\left(g\right)\)
Vậy ...

Số OXH của Fe sau khi tác dụng với dung dịch HCl là +2 còn sau khi td với Cl2 là +3
TN1
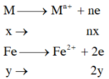
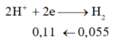
=> nx+2y=0,11 (1)
TN2: Xét cả quá trình
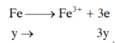
=> nx+3y=0,12 (2)
(1)-(2) được y=0,01
Thay y=0,01 vào (2) được nx=0,09(3)
Lại có: 56.0,01+ xM=1,37
=> Mx=0,81 (4)
(3)(4)=> M=9n
=> Kim loại là Al
Đáp án C





47.
Đặt \(n_{KClO_3}=c\left(mol\right)\)
\(n_{KCl}=0,2\left(mol\right)\)
\(BTNT.Cr\Rightarrow n_{K_2Cr_2O_7}=\frac{1}{2}n_{CrCl_3}=0,5b\left(mol\right)\\ BTNT.Mn\Rightarrow n_{KMnO_4}=n_{MnCl_2}=a\left(mol\right)\\ \Rightarrow m_X=158x+122,5c+147b=57,45\left(1\right)\\ BTNT.K\Rightarrow n_{KCl}=n_{KMnO_4}+n_{KClO_3}+2n_{K_2Cr_2O_7}\\ =a+b+c=0,4\left(2\right)\\ \text{Mà }2a=b\left(3\right)\)
\(\left(1\right);\left(2\right);\left(3\right)\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,2\\c=0,1\end{matrix}\right.\)
QT nhường e:
Mn+7 + 5e ----> Mn+2
0,1_____0,5
Cl+5 + 6e ----> Cl-
0,1____0,6
Cr2+6 + 6e ----> 2Cr+3
_______0,6______0,2
QT nhận e: 2Cl- ----> Cl2 + 2e
BT e \(\Rightarrow n_{Cl_2}=0,85\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=19,04\left(l\right)\)
Bài 47:
Gọi số mol KMnO4; KClO3; K2Cr2O7 lần lượt là x, y, z.
\(\Rightarrow158x+122,5y+294z=57,45\)
Phản ứng xảy ra:
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
\(K_2Cr_2O_7+14HCl\rightarrow2KCl+2CrCl_3+3Cl_2+7H_2O\)
\(\Rightarrow n_{KCl}=n_{KMnO4}+n_{KClO3}+2n_{K2Cr2O7}=x+y+2z=\frac{29,8}{39+35,5}=0,4\left(mol\right)\)
\(n_{MnCl2}=n_{KMnO4}=x;n_{CrCl3}=n_{K2Cr2O7}=z=2x\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,0633\\y=0,0835\\z=0,1266\end{matrix}\right.\)
\(\Rightarrow n_{Cl2}=\frac{5}{2}n_{KMnO4}+3n_{KClO3}+3n_{K2Cr2O7}\)
\(=2,5x+3y+3z=0,78855\left(mol\right)\)
\(\Rightarrow V=0,78855.22,4=17,66352\left(l\right)\)