Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


BTKL: mD + mNaHCO3 = mCO2 + mE
mD + 179,88 = 44.0,2 + 492 => mD = 320,92
BTKL: mMg + mddHCl = mH2 + mD
=> 24 . 0,4 + mddHCl = 2 . 0,4 + 320,92 => mddHCl = 312,12
=> C%HCl = 11,69%

Gọi n là hóa trị của M
Phản ứng xảy ra:
4M+nO2→2M2On
Giả sử số mol M là 1 mol.
→nM2On=1/2nM=0,5 mol
→mM=m=1M(M)=M(M)gam
mM2On=0,5.(2MM+16MO)=0,5(2MM+16n)=MM+8n=1,25m
→MM+8n=1,25MM→MM=32n→n=2→MM=64→M:Cu(Đồng)
Hòa tan oxit
CuO+H2SO4→CuSO4+H2O
Ta có:
mH2SO4=200.19,6%=39,2 gam
→nH2SO4=39,298=0,4 mol = nCuO=nCuSO4
→mCuO=0,4.(64+16)=32 gam;mCuSO4=0,4.(64+96)=64 gam
Áp dụng định luật bảo toàn khối lượng:
mddX=mCuO+mddH2SO4=200+32=232 gam
→C%CuSO4=64232=27,5862%
chúc bạn học tốt
Gọi n là hóa trị của M Phản ứng xảy ra: 4M+nO2→2M2On
Giả sử số mol M là 1 mol.
→nM2On=1/2nM=0,5 mol →mM=m=1M(M)=M(M)gam
mM2On=0,5.(2MM+16MO)=0,5(2MM+16n)=MM+8n=1,25m →MM+8n=1,25MM→MM=32n→n=2→MM=64→M:Cu(Đồng)

Giả sử kim loại hóa trị II là A.
Ta có: nBa(OH)2 = 0,1 (mol)
nBaCO3 = 0,05 (mol)
\(ACO_3\underrightarrow{t^o}AO+CO_2\)
- TH1: Ba(OH)2 dư.
PT: \(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
Theo PT: \(n_{ACO_3}=n_{CO_2}=n_{BaCO_3}=0,05\left(mol\right)\)
\(\Rightarrow M_{ACO_3}=\dfrac{15}{0,05}=300\left(g/mol\right)\Rightarrow M_A=240\left(g/mol\right)\)
→ Không có chất nào thỏa mãn.
- TH2: Ba(OH)2 hết.
PT: \(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
______0,05_____0,05_____0,05 (mol)
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\)
___0,05_____0,1 (mol)
⇒ nCO2 = 0,05 + 0,1 = 0,15 (mol)
Theo PT: \(n_{ACO_3}=n_{CO_2}=0,15\left(mol\right)\Rightarrow M_A=\dfrac{15}{0,15}=100\left(g/mol\right)\)
\(\Rightarrow M_A=40\left(g/mol\right)\)
→ A là Ca.
Vậy: CTHH cần tìm là CaCO3

a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
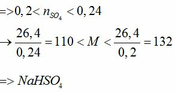
b)
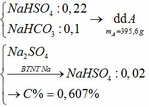
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O

a, PT: \(MO+CO\underrightarrow{t^o}M+CO_2\)
Ta có: \(n_{MO}=\dfrac{7,2}{M_M+16}\left(mol\right)\)
\(n_M=\dfrac{5,6}{M_M}\left(mol\right)\)
Theo PT: \(n_{MO}=n_M\) \(\Rightarrow\dfrac{7,2}{M_M+16}=\dfrac{5,6}{M_M}\)
\(\Rightarrow M_M=56\left(g/mol\right)\)
⇒ M là Fe.
Vậy: Oxit kim loại đó là FeO.
b, Theo PT: \(n_{CO_2}=n_M=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{\downarrow}=m_{CaCO_3}=0,1.100=10\left(g\right)\)
Bạn tham khảo nhé!






Lấy 7,11 gam phèn nung tới khối lượng không đổi thì thu được 3,87 gam phèn khan. => Khối lượng nước ở trong phèn là:
mH2O(.)phèn = 7,11 – 3,87 = 3,24(g)
Số mol nước ở trong phèn: nH2O(.) phèn = 3,24/18 = 0,18 (mol)
Số mol kết tủa BaSO4: nBaSO4 = 6,99/233 = 0,03 (mol)
Ta có: Số mol phèn = ½ số mol của kết tủa
BaSO4 = ½ x 0,03 = 0,015 (mol)
Do đó khối lượng mol của phèn là: M phèn = 7,11/0,015 = 474(g)
Vì số mol của H2O trong phèn là 0,18 và số mol của phèn là 0,015 nên ta có phương trình: 0,015n = 0,18. Giải ra được: n = 12.
Do đó khối lượng của kim loại M trong phèn là:
MM = 474 – 27 - 12x18 – 96x2 = 39 (g) => M là Kali
(thỏa mãn là kim loại thuộc nhóm IA bảng tuần hoàn các NTHH).
Kết luận: Vậy CTPT của phèn là : KAl(SO4)2.12H2O.