2. Hòa tan Ba(OH)2 vào nước được 800 ml Ba(OH)2 0,2M. Tính khối lượng của Ba(OH)2 có trong dung dịch

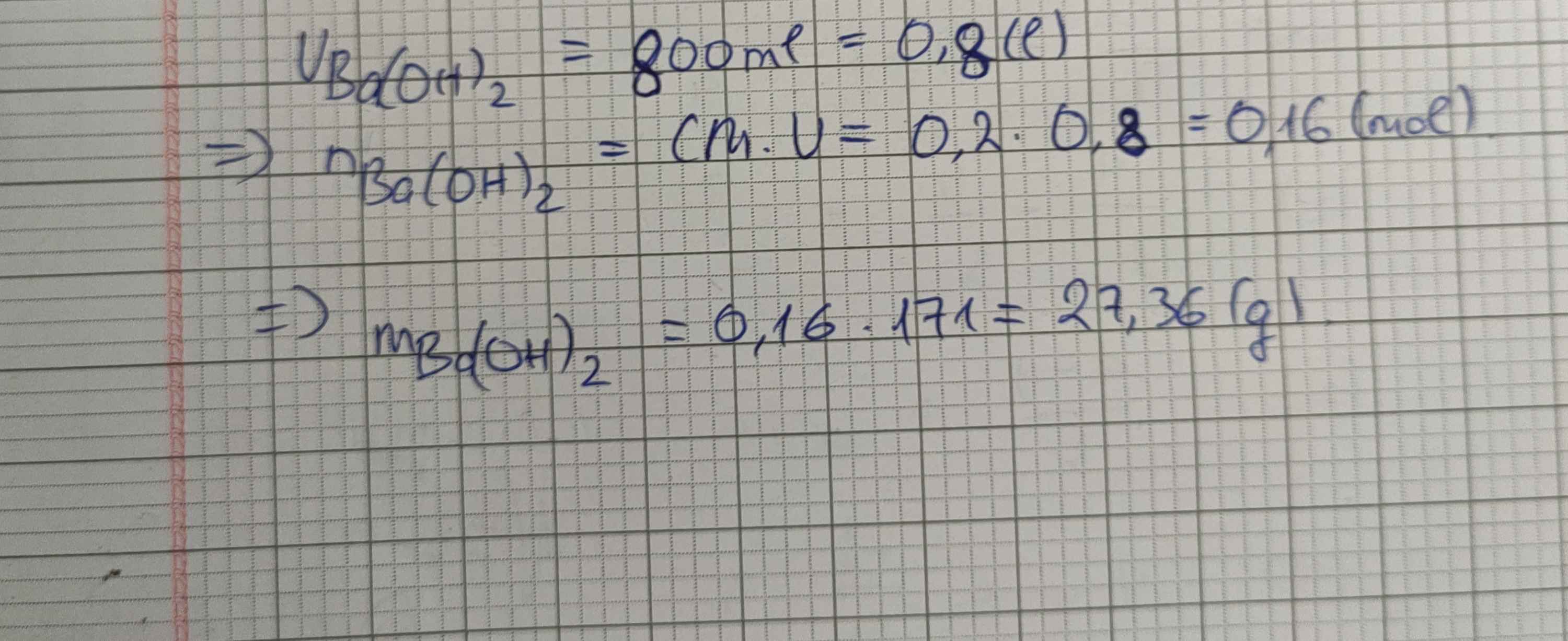
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
2. Hòa tan Ba(OH)2 vào nước được 800 ml Ba(OH)2 0,2M. Tính khối lượng của Ba(OH)2 có trong dung dịch

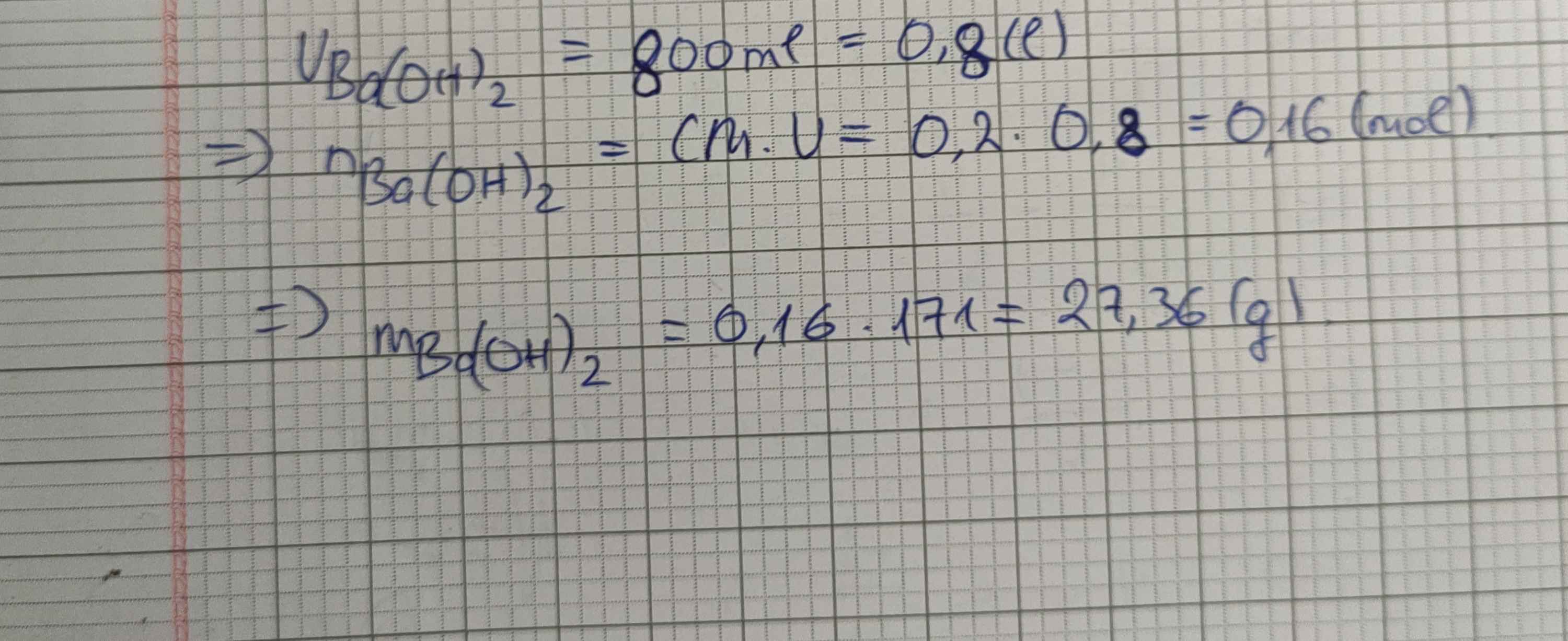

nBa(OH)2 = 0,4.0,3 = 0,12 mol
mBa(OH)2 = 0,12.171 = 20,52g
300ml=0.3l
nBa(OH)2= CM × V= 0.4×0.3= 0.12 (mol)
mBa(OH)2= n×M= 0.12× 171=20.52 (g)

$n_{Ba} = n_{Ba(OH)_2} = 0,12(mol)$
$n_{H_2} = \dfrac{1,12}{22,4} = 0,05(mol)$
Gọi $n_{Na} = a ; n_O = b$
Ta có :
$23a + 16b + 0,12.137 = 21,1$
Bảo toàn electron : $a + 0,12.2 = 2b + 0,05.2$
Suy ra $a = \dfrac{177}{1550} ; b = \dfrac{197}{1550}$
Suy ra $m_{NaOH} = \dfrac{177}{1550}.40 = 4,57(gam)$

PT: \(2K+2H_2O\rightarrow2KOH+H_2\)
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(K_2O+H_2O\rightarrow2KOH\)
\(BaO+H_2O\rightarrow Ba\left(OH\right)_2\)
Ta có: \(n_{H_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
Theo PT, có: \(\Sigma n_{H_2}=\dfrac{1}{2}n_K+n_{Ba}\)
\(\Rightarrow n_K+2n_{Ba}=0,04\left(1\right)\)
Ta có: \(n_{KOH}=\dfrac{2,24}{56}=0,04\left(mol\right)\)
Theo PT: \(\Sigma n_{KOH}=n_K+2n_{K_2O}\)
\(\Rightarrow n_K+2n_{K_2O}=0,04\left(2\right)\)
Từ (1) và (2) \(\Rightarrow n_K+2n_{Ba}=n_K+2n_{K_2O}\) \(\Rightarrow n_{Ba}=n_{K_2O}=\dfrac{0,04-n_K}{2}\) (3)
Mà: mA = 4,62 (g)
\(\Rightarrow39n_K+137n_{Ba}+94n_{K_2O}+153n_{BaO}=4,62\) (4)
Từ (3) và (4) \(\Rightarrow2n_{BaO}=n_K\) (5)
Từ (1) và (5) \(\Rightarrow n_{BaO}+n_{Ba}=\dfrac{0,04}{2}=0,02\left(mol\right)\)
Theo PT: \(\Sigma n_{Ba\left(OH\right)_2}=n_{Ba}+n_{BaO}=0,02\left(mol\right)\)
\(\Rightarrow m_{Ba\left(OH\right)_2}=0,02.171=3,42\left(g\right)\)
Tuy cách này vận dụng toán nhiều hơn hóa nhưng bạn tham khảo nhé!
Coi A gồm : K,Ba,O
Ta có : \(n_K = n_{KOH} = \dfrac{2,24}{56} = 0,04(mol)\)
Gọi :\(\left\{{}\begin{matrix}n_{Ba}=a\left(mol\right)\\n_O=b\left(mol\right)\end{matrix}\right.\)⇒ 137a + 16b = 4,62 - 0,04.39 = 3,06(1)
Bảo toàn e :
\(n_K + 2n_{Ba} = 2n_{H_2} + 2n_O\\ \Rightarrow 2a - 2b = 0(2)\)
Từ (1)(2) suy ra a = 0,02 ; b = 0,02
Vậy :
\(n_{Ba(OH)_2} = n_{Ba} = 0,02(mol)\\ \Rightarrow m_{Ba(OH)_2} = 0,02.171 = 3,42(gam)\)

a)
Gọi thể tích hai bazo là V
Suy ra :
n NaOH = 0,1V ; n Ba(OH)2 = 0,15V
n HCl = 0,2.0,2 = 0,04(mol) ; n H2SO4 = 0,2.0,1 = 0,02(mol)
Bản chất của phản ứng là H trong axit tác dụng với OH trong bazo tạo thành nước :
$H + OH \to H_2O$
n H = n HCl + 2n H2SO4 = 0,08(mol)
n OH = n NaOH + 2n Ba(OH)2 = 0,4V
Theo PTHH :
n H = n OH <=> 0,08 = 0,4V <=> V = 0,2(lít)
b) Dung dịch sau pư có :
Na+ : 0,02
Ba2+ :
Cl- : 0,04
Bảo toàn điện tích => n Ba2+ = 0,01(mol)
=> n BaSO4 = n Ba(OH)2 - n Ba2+ = 0,03 - 0,01 = 0,02
m BaSO4 = 0,02.233 = 4,66 gam
vì sao lại có đoạn này vậy ạ :
n H = n HCl + 2n H2SO4 = 0,08(mol)

\(n_{Ba\left(OH\right)_2}=0,5.0,2=0,1\left(mol\right)\)
PTHH: Ba(OH)2 + 2HCl -----> BaCl2 + 2H2O
Mol: 0,1 0,2
\(m_{HCl}=0,2.36,5=7,3\left(g\right)\Rightarrow m_{ddHCl}=\dfrac{7,3.100\%}{15\%}=\dfrac{146}{3}\left(g\right)\)
\(\Rightarrow V_{ddHCl}=\dfrac{\dfrac{146}{3}}{1,25}=\dfrac{584}{15}=38,9\left(ml\right)\)