Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cho các phát biểu sau
(1) Dãy HF, HCl, HBr, HI: độ bền tăng dần, tính axit và tính khử tăng dần.
(2) HF là axit yếu nhưng có tính chất đặc biệt ăn mòn thủy tinh.
(3) Phản ứng: NaX (tt) + H2SO4 đặc
(4) Các muối AgX đều là chất kết tủa (X là halogen).
(5) Không thể bảo quản axit HF trong chai, lo bằng thủy tinh.
(6) Trong nhóm halogen, theo chiều tăng dần điện tích hạt nhân: tính phi kim (tính oxy hóa) giảm dần còn tính khử tăng dần.
(7) Trong phòng thí nghiệm, có thể điều chế clo bằng cách cho HCl đặc tác dụng với các chất oxi hóa mạnh như MnO2, KMnO4, KClO3, K2Cr2O7,…
(8) Trong công nghiệp, điều chế clo bằng cách điện phân dung dịch natri clorua NaCl bão hòa (không có màng ngăn) .
Số phát biểu đúng là A. 2. B. 3. C. 4. D.5

Câu 1: Cho dãy dung dịch axit sau HF, HCl, HBr, HI. Dung dịch có tính axit mạnh nhất và tính khử mạnh nhất là:
A. HF
B. HCl
C. HBr
D. HI
Giải thích: Tính khử, tính axit tăng dần theo thứ tự: HF < HCl < HBr < HI
Câu 2: Nung 8,1gam bột nhôm với 38,1gam iot , biết hiệu suất phản ứng là 80%. Lượng Iotua nhôm thu được là :
A. 81,6g
B. 97,92g
C. 65,28g
D. 102g
Giải thích:
\(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\); \(n_{I_2}=\dfrac{38,1}{254}=0,15\left(mol\right)\)
PTHH: 2Al + 3I2 --H2O--> 2AlI3
Xét tỉ lệ: \(\dfrac{0,3}{2}>\dfrac{0,15}{3}\) => Hiệu suất tính theo I2
\(n_{I_2\left(pư\right)}=\dfrac{0,15.80}{100}=0,12\left(mol\right)\)
PTHH: 2Al + 3I2 --H2O--> 2AlI3
0,12------->0,08
=> mAlI3 = 0,08.408 = 32,64 (g)
=> Không có đáp án thỏa mãn
Câu 3: Khi sục chất khí nào sau đây vào dung dịch KI có hồ tinh bột thì sau phản ứng dung dịch có màu xanh:
A. Cl2
B. O3
C. O2
D. Cl2, O3
Giải thích:
2KI + Cl2 --> 2KCl + I2
2KI + O3 + H2O --> 2KOH + I2 + O2
I2 làm xanh dd hồ tinh bột
Câu 4: Cho NaI rắn vào bình dung dịch H2SO4đđ nóng dư. Sau khi phản ứng kết thúc thêm vài giọt hồ tinh bột vào bình phản ứng thì dung dịch sẽ có màu:
A. Nâu
B. Đỏ
C. Tím
D. Xanh
2NaI + 2H2SO4 --> Na2SO4 + SO2 + I2 + 2H2O
I2 làm xanh dd hồ tinh bột
Câu 5: Tính oxi hóa của Br2:
A. mạnh hơn Flo nhưng yếu hơn Clo.
B. mạnh hơn Clo nhưng yếu hơn Iot.
C. mạnh hơn Iot nhưng yếu hơn Clo.
D. mạnh hơn Flo nhưng yếu hơn Iot.
Giải thích: Tính oxh tăng dần theo thứ tự: I2 < Br2 < Cl2 < F2
Câu 6: Trong phản ứng hóa học sau, Brom đóng vai trò là SO2 + Br2 + 2H2O H2SO4 + 2HBr
A. Chất khử.
B.Vừa là chất oxi hóa vừa là chất khử.
C.Chất oxi hóa.
D.Không là chất oxi hóa không là chất khử.
Giả thích: Br0 bị khử xuống Br-1 => Br2 là chất oxh
Câu 7: Chất khí có thể làm mất màu dung dịch nước Brom là:
A. SO2.
B. CO2.
C. O2.
D. HCl.
Giải thích: SO2 + Br2 + 2H2O --> 2HBr + H2SO4
Câu 8: Đổ dd chứa 1 g HBr vào dd chứa 1 g NaOH. Nhúng giấy quì tím vào dung dịch thu được thì giấy quì tím chuyển sang màu: A
. Màu đỏ.
B. Màu xanh.
C. Không màu.
D. Màu tím.
Giải thích:
\(n_{HBr}=\dfrac{1}{81}\left(mol\right)\); \(n_{NaOH}=\dfrac{1}{40}=0,025\left(mol\right)\)
PTHH: NaOH + HBr --> NaBr + H2O
Xét tỉ lệ: \(\dfrac{\dfrac{1}{81}}{1}< \dfrac{0,025}{1}\) => NaOH dư => QT chuyển xanh
Câu 9: Chất A là muối Canxi halogenua. Dung dịch chứa 0.200 g A tác dụng với lượng dư dung dịch bạc nitrat thì thu được 0.376 g kết tủa bạc halogenua. Công thức phân tử của chất A là:
A. CaF2.
B. CaCl2.
C. CaBr2.
D. CaI2.
Giải thích:
nCaX2 = \(\dfrac{0,2}{40+2.M_X}\) (mol)
=> nAgX = \(\dfrac{0,2}{20+M_X}\) (mol)
=> \(M_{AgX}=\dfrac{0,376}{\dfrac{0,2}{20+M_X}}=1,88\left(20+M_X\right)\)
=> MX = 80 (g/mol)
=> X là Br
=> CTHH: CaBr2
Câu 10: Phát biểu nào sau đây không chính xác:
A. Halogen là những phi kim điển hình, chúng là những chất oxi hóa.
B. Trong hợp chất các halogen đều có thể có số oxi hóa: -1, +1, +3, +5, +7.
C. Khả năng oxi hóa của halogen giảm dần từ flo đến iot
D. Các halogen khá giống nhau về tính chất hóa học.
Giải thích: B sai do Flo chỉ có số oxi hóa là -1
Câu 1: Cho dãy dung dịch axit sau HF, HCl, HBr, HI. Dung dịch có tính axit mạnh nhất và tính khử mạnh nhất là:
A. HF
B. HCl
C. HBr
D. HI
Câu 2: Nung 8,1gam bột nhôm với 38,1gam iot , biết hiệu suất phản ứng là 80%. Lượng Iotua nhôm thu được là :
A. 81,6g
B. 97,92g
C. 65,28g
D. 102g
Câu 3: Khi sục chất khí nào sau đây vào dung dịch KI có hồ tinh bột thì sau phản ứng dung dịch có màu xanh:
A. Cl2
B. O3
C. O2
D. Cl2, O3
Câu 4: Cho NaI rắn vào bình dung dịch H2SO4đđ nóng dư. Sau khi phản ứng kết thúc thêm vài giọt hồ tinh bột vào bình phản ứng thì dung dịch sẽ có màu:
A. Nâu
B. Đỏ
C. Tím
D. Xanh
Câu 5: Tính oxi hóa của Br2:
A. mạnh hơn Flo nhưng yếu hơn Clo.
B. mạnh hơn Clo nhưng yếu hơn Iot.
C. mạnh hơn Iot nhưng yếu hơn Clo.
D. mạnh hơn Flo nhưng yếu hơn Iot.
Câu 6: Trong phản ứng hóa học sau, Brom đóng vai trò là SO2 + Br2 + 2H2O H2SO4 + 2HBr
A. Chất khử.
B.Vừa là chất oxi hóa vừa là chất khử.
C.Chất oxi hóa.
D.Không là chất oxi hóa không là chất khử.
Câu 7: Chất khí có thể làm mất màu dung dịch nước Brom là:
A. SO2.
B. CO2.
C. O2.
D. HCl.
Câu 8: Đổ dd chứa 1 g HBr vào dd chứa 1 g NaOH. Nhúng giấy quì tím vào dung dịch thu được thì giấy quì tím chuyển sang màu: A
. Màu đỏ.
B. Màu xanh.
C. Không màu.
D. Màu tím.
Câu 9: Chất A là muối Canxi halogenua. Dung dịch chứa 0.200 g A tác dụng với lượng dư dung dịch bạc nitrat thì thu được 0.376 g kết tủa bạc halogenua. Công thức phân tử của chất A là:
A. CaF2.
B. CaCl2.
C. CaBr2.
D. CaI2.
Câu 10: Phát biểu nào sau đây không chính xác:
A. Halogen là những phi kim điển hình, chúng là những chất oxi hóa.
B. Trong hợp chất các halogen đều có thể có số oxi hóa: -1, +1, +3, +5, +7.
C. Khả năng oxi hóa của halogen giảm dần từ flo đến iot
D. Các halogen khá giống nhau về tính chất hóa học.

Tính oxi hóa giảm dần từ F2 đến I2.
- Flo là phi kim mạnh nhất, oxi hóa được tất cả các kim loại kể cả vàng và platin. Clo, Br và Iot tác dụng được với một số kim loại.
- Phản ứng với hiđro.

- Halogen đứng trước đẩy halogen đứng sau ra khỏi muối của chúng:
Cl2 + 2NaBr → 2NaCl + Br2
Br2 + 2NaI → 2NaBr + I2
Tính khử của axit tăng theo chiều: HF < HCl < HBr < HI.
- Chỉ có thể oxi hóa F- bằng dòng điện. Còn ion Cl-, Br-, I- đều có thể bị oxi hóa khi tác dụng với chất oxi hóa mạnh.
- HF hoàn toàn không thể hiện tính khử, HCl chỉ thể hiện tính khử khi tác dụng với những chất oxi hóa mạnh, còn HBr và nhất là HI có tính khử mạnh. Axit sunfuric đặc bị HBr khử đến SO2 và bị HI khử đến H2S:
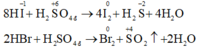

Chọn đáp án B
1. Đúng.
2. Sai.HF là axit rất yếu.Ăn mòn thủy tinh là tính chất riêng có.
3. Sai.Tính khử và tính axit tăng dần
4. Sai điều chế bằng điện phân dung dịch NaCl không có màng ngăn.
5. Sai HClO là axit rất yếu

Câu 24: Cho các phát biểu sau:
(1). Dung dịch 5% iot trong etanol dùng làm thuốc sát trùng vết thương.✔
(2). Dãy axit HF, HCl, HBr, HI được sắp xếp theo chiều tính khử tăng dần.✖
(3). Khí oxi và ozon đều là chất oxi hoá mạnh, tính oxi hoá của khí ozon mạnh hơn khí oxi.✔
(4). Khí clo, khí oxi và khí ozon đều được dùng để diêt trùng nước sinh hoạt.✖
(5). Cho dung dịch AgNO3 dư vào dung dịch chứa NaF, NaCl thu được hai chất kết tủa .✖
Số nhận định đúng là
A. 1. B. 2. C. 3. D. 4.
Câu 25: Hỗn hợp khí X gồm ozon và oxi có tỉ khối đối với hiđro bằng 20,8. Phần trăm theo thể tích ozon và oxi trong hỗn hợp X lần lượt là
A. 60% và 40%. B. 30% và 70%. C. 35% và 65%. D. 40% và 60%.
Câu 26: Cho 19,3 gam bột hỗn hợp Fe và Al đun nóng với S dư, sau khi phản ứng xảy ra hoàn toàn thu được 40,1 gam hỗn hợp muối. Thành phần % theo số mol của Fe trong hỗn hợp ban đầu là
A. 50,00%. B. 67,47%. C. 45,00% D. 40,00%
Đáp án: \(58,03\%\)

Điều chế HF, HCl bằng cách cho H 2 SO 4 đặc tác dụng với muối florua, clorua vì H 2 SO 4 à chất oxi hoá không đủ mạnh để oxi hoá được HF và HCl. Nói cách khác, HF và HCl có tính khử yếu, chúng không khử được H 2 SO 4 đặc
Ca F 2 + H 2 SO 4 → Ca SO 4 + 2HF
NaCl + H 2 SO 4 → NaH SO 4 + HCl
Nhưng không thể dùng phương pháp trên để điều chế HBr và HI vì H 2 SO 4 đặc oxi hoá được những chất này thành Br 2 và I 2 . Nói cách khác, HBr và HI là những chất có tính khử mạnh hơn HCl và HF.
NaBr + H 2 SO 4 → HBr + NaH SO 4
2HBr + H 2 SO 4 → Br 2 + SO 2 + 2 H 2 O
NaI + H 2 SO 4 → NaH SO 4 + HI
2HI + H 2 SO 4 → I 2 + SO 2 + 2 H 2 O