Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
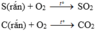
Từ 2 phương trình trên ta thấy số mol khí của chất tham gia phản ứng và sau phản ứng bằng nhau và không phụ thuộc vào lượng C, S => do vậy áp suất của bình sẽ không thay đổi khi ta đưa về nhiệt độ ban đầu

\(\dfrac{mH2}{mO2}\)=\(\dfrac{3}{8}\)=x
=>;mH2=x=>nH2=\(\dfrac{3x}{2}\)mol
m02=\(\dfrac{8x}{32}\)=\(\dfrac{x}{4}\)mol
PTHH: 2H2 + O2 to→ 2H2O
xét: \(\dfrac{3x}{2}\);\(\dfrac{3x}{12}\)
h2 dư, o2 hết
nh2dư=\(\dfrac{3x}{2}-\dfrac{3x}{12}\)\(=\dfrac{15x}{12}\)=\(\dfrac{1,792}{22,4}\)=0,08(mol)
=>x=\(\dfrac{0,08.12}{15}\)=0,064
nO2=\(\dfrac{0,064}{4}\)=0,016(mol)
nH2=\(\dfrac{0,064.3}{2}\)=0,096(mol)
VQ(đktc)=22,4(0,016+0,096)=2,5088(lít)

Gọi số mol H2, O2 là a, b (mol)
Ta có: \(\dfrac{m_{H_2}}{m_{O_2}}=\dfrac{3}{8}\)
=> \(\dfrac{2a}{32b}=\dfrac{3}{8}\Rightarrow\dfrac{a}{b}=\dfrac{6}{1}\) hay a = 6b
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{6b}{2}>\dfrac{b}{1}\) => H2 dư, O2 hết
PTHH: 2H2 + O2 --to--> 2H2O
2b<---b
=> \(n_{H_2\left(dư\right)}=6b-2b=4b=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
=> b = 0,02 (mol)
=> a = 0,12 (mol)
=> VQ = (0,02 + 0,12).22,4 = 3,136 (l)
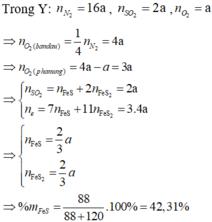
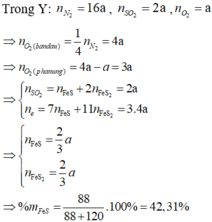
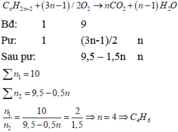
a, Áp suất trong bình không thay đổi vì quá trình đốt cháy lưu huỳnh trong hỗn hợp X là quá trình xảy ra ở áp suất không đổi và sau khi đốt cháy, các sản phẩm khí sinh ra có cùng nhiệt độ và áp suất với hỗn hợp ban đầu.
b,Để tính phần trăm thể tích của hỗn hợp khí Y, ta cần biết tỉ lệ mol của các khí trong hỗn hợp Y. Theo phương trình phản ứng, khi đốt cháy lưu huỳnh trong hỗn hợp X, ta có:
S + O2 → SO2
Vì tỉ lệ mol giữa N2, O2 và SO2 trong hỗn hợp X là 2:1:1 nên khi đốt cháy hết lưu huỳnh, tỉ lệ mol giữa N2 và O2 trong hỗn hợp Y sẽ là 2:5. Do đó, ta có:
Tổng số mol khí trong hỗn hợp Y: 2 + 5 = 7 (vì tỉ lệ mol giữa N2 và O2 là 2:5)
Phần trăm thể tích của hỗn hợp Y: \(d\dfrac{Y}{X}\) = \(\dfrac{V_Y}{V_X}\) = \(\dfrac{n_Y.\dfrac{RT}{P}}{n_X.\dfrac{RT}{P}}=\dfrac{n_Y}{n_X}\) = 7/4 ≈ 175%
Vậy phần trăm thể tích của hỗn hợp khí Y là khoảng 175%.
c, Ta có:
\(d\dfrac{Y}{X}=\dfrac{V_Y}{V_X}=\dfrac{n_Y.\dfrac{RT}{P}}{n_X.\dfrac{RT}{P}}=\dfrac{n_Y}{n_X}\)
Với mỗi mol lưu huỳnh đốt cháy, số mol khí trong hỗn hợp Y tăng thêm 2, do đó nY = nX + 2 nhân số mol lưu huỳnh đốt cháy.
Từ đó suy ra: dY/X = (nX + 2 . số mol lưu huỳnh đốt cháy) / nX = 1 + 2 . số mol lưu huỳnh đốt cháy / nX
Do đó:
1 dY/X 1,21 tương đương với (dY/X) / 1,1684 = 1 + 2 . số mol lưu huỳnh đốt cháy / nX / 1,1684
=> 1,21 / 1,1684 - 1 = 2 . số mol lưu huỳnh đốt cháy / nX
=> số mol lưu huỳnh đốt cháy / nX = 0,0217
=> số mol lưu huỳnh đốt cháy = 0,0217 . nX
Vậy khi lượng lưu huỳnh biến đổi, 1 dY/X tăng thêm 2 . 0,0217 = 0,0434.