Cho m gam tinh bột lên men thành C2H5OH với hiệu suất 81%, hấp thụ hết lượng CO2 sinh ra vào dung dịch Ca(OH)2 được 55 gam kết tủa và dung dịch X. Đun nóng dung dịch X lại có 10 gam kết tủa nữa. Giá trị m là:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Hướng dẫn:
C6H12O6 → 2CO2 + 2C2H5OH
Ca(OH)2 + CO2 → CaCO3 + 2H2O
nCaCO3 = 0,55 mol ; nCa(HCO3)2 = 0,1 mol
=> nCO2 = 0,75 mol
=> ntinh bột = 0,75.100/81 = 0,925 mol
=> m = 0,925.162 = 150 g

\(n_{CaCO_3\left(1\right)}=\dfrac{m_{CaCO_3}}{M_{CaCO_3}}=\dfrac{55}{100}=0,55\left(mol\right)\)
\(n_{CaCO_3\left(2\right)}=0,1\left(mol\right)\Rightarrow n_{Ca\left(HCO_3\right)_2}=0,1\left(mol\right)\)
Bảo toàn nguyên tố C:
\(n_{CO_2}=n_{CaCO_3\left(1\right)}+2n_{Ca\left(HCO_3\right)_2}=0,55+2.0,1=0,75\left(mol\right)\)
\(\left(C_6H_{10}O_5\right)_n\rightarrow C_6H_{12}O_6\rightarrow2C_2H_5OH+2CO_2\)\(n_{\text{tb(phản ứng) }}=\dfrac{1}{2}n_{CO_2}=\dfrac{1}{2}0,75=0,375\left(mol\right)\)
\(H=\dfrac{m_{tt}}{m_{lt}}.100\%\Leftrightarrow m_{lt}=\dfrac{m_{tt}}{H}.100\%=\dfrac{0,375.162}{80}.100\%=75\left(g\right)\)


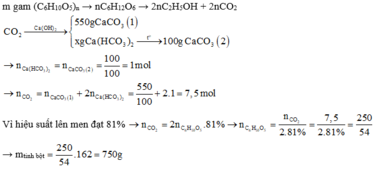
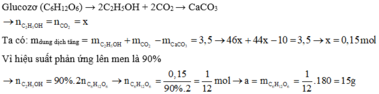
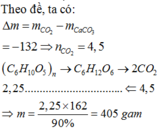
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O(1)$
$2CO_2 + Ca(OH)_2 \to Ca(HCO_3)_2 (2)$
$Ca(HCO_3)_2 \xrightarrow{t^o} CaCO_3 + CO_2 + H_2O(3)$
$n_{CaCO_3(1)} = 0,55(mol)$
$n_{Ca(HCO_3)_2} = n_{CaCO_3(3)} = 0,1(mol)$
$\Rightarrow n_{CO_2} = n_{CaCO_3} + 2n_{Ca(HCO_3)_2} = 0,75(mol)$
$(C_6H_{10}O_5)_n + nH_2O \xrightarrow{xt,t^o} nC_6H_{12}O_6$
$C_6H_{12}O_6 \xrightarrow{xt,t^o} 2CO_2 + 2C_2H_5OH$
$n_{tinh\ bột\ pư} = \dfrac{1}{2n}n_{CO_2} = \dfrac{0,375}{n}(mol)$
$n_{tinh\ bột\ đã\ dùng} = \dfrac{0,375}{n} : 81\% = \dfrac{25}{54n}(mol)$
$m = \dfrac{25}{54n}.162n = 75(gam)$
Nói v ai chả nói đc ba