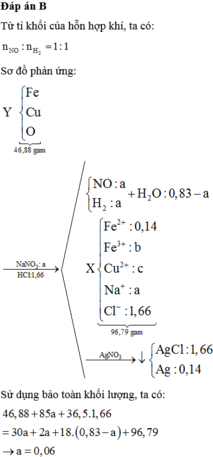
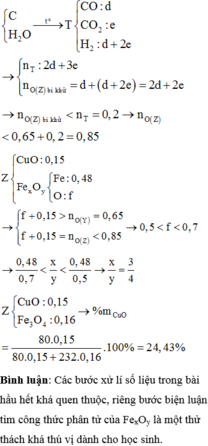cho 19,5 gam Zn tác dụng với dung dịch loãng có chứa 39,2 gam axit sunfuric
a) tính thể tích H2 thu đc.
b)dẫn toàn bộ khí thu đc ở trên qua hỗn hợp A gồm CuO và Fe3O4 nung nóng thì thấy khối lượng hỗn hợp A giảm đi m gam.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a/ \(Zn+H_2SO_{4_{loãng}}\rightarrow ZnSO_4+H_2\)
b/ \(n_{Zn}=0,3\left(mol\right)\\ n_{H_2SO_4}=0,4\left(mol\right)\)
Vì ta có tỉ lệ \(\dfrac{n_{Zn}}{1}< \dfrac{n_{H_2SO_4}}{1}\) nên \(H_2SO_4\) dư
\(n_{H_2}=0,3\left(mol\right)\\ V_{H_2}=0,3\times22,4=6,72\left(lít\right)\)

nZn=\(\frac{19,5}{65}=0,3\)mol
2Zn+2Hcl--->2Zncl+H2
pt:2mol 2mol 2mol 1mol
bt:0,3mol xmol
=>x=\(\frac{0,3.1}{2}=0,15\)mol
áp dụng:V=n.22,4=>VH2=0,15.22,4=3,36 lít
ai tích mk mk sse tích lại

a, \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Xét tỉ lệ: \(\dfrac{0,25}{1}< \dfrac{0,3}{1}\), ta được H2SO4 dư.
Theo PT: \(n_{H_2}=n_{Fe}=0,25\left(mol\right)\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)
b, \(H_2+O_{\left(trongoxit\right)}\rightarrow H_2O\)
\(n_{O\left(trongoxit\right)}=n_{H_2}=0,25\left(mol\right)\)
Có: mX giảm = mO (trong oxit) = 0,25.16 = 4 (g) = a

a.b.\(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{2,7}{27}=0,1mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1 0,15 ( mol )
\(V_{H_2}=n_{H_2}.22,4=0,15.22,4=3,36l\)
c.\(n_{CuO}=\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{16}{80}=0,2mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,2 < 0,15 ( mol )
0,15 0,15 0,15 ( mol )
\(m_A=m_{CuO\left(dư\right)}+m_{Cu}=\left[\left(0,2-0,15\right).80\right]+\left[0,15.64\right]=4+9,6=13,6g\)

PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\) (1)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\) (2)
a) Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\) \(\Rightarrow n_{HCl\left(1\right)}=0,6mol\)
Theo PTHH: \(n_{Zn}=n_{H_2}=0,3mol\) \(\Rightarrow m_{Zn}=0,3\cdot65=19,5\left(g\right)\)
\(\Rightarrow m_{Fe_2O_3}=16\left(g\right)\) \(\Rightarrow n_{HCl\left(2\right)}=6n_{Fe_2O_3}=6\cdot\dfrac{16}{160}=0,6\left(mol\right)\)
\(\Rightarrow\Sigma n_{HCl}=1,2mol\)
*Bạn cần bổ sung thêm nồng độ % dd HCl
Đề bài chỉ yêu cầu tính khối lượng axit chứ đâu có yêu cầu tính khối lượng dung dịch axit nhỉ?

a)
Zn + 2HCl → ZnCl2 + H2 (1)
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (2)
nH2 = \(\dfrac{6,72}{22,4}\)= 0,3 mol
Theo (1) => nZn = nH2 = 0,3mol => nHCl phản ứng ở (1) = 0,3.2 =0,6mol
mZn = 0,3.65 = 19,5 gam => mFe2O3 = 35,5 - 19,5 = 16 gam
<=> nFe2O3 = \(\dfrac{16}{160}\)=0,1 mol => nHCl phản ứng ở (2) = 0,1.6 = 0,6 mol
=> nHCl phản ứng = 0,6 + 0,6 = 1,2 mol <=> mHCl phản ứng = 0,6.36,5 =21,9 gam
b) nH2 = 0,3 mol , hiệu suất phản ứng = 60% => nH2 phản ứng = 0,3.60% = 0,18 mol
H2 + \(\left\{{}\begin{matrix}CuO\\Fe3O4\end{matrix}\right.\) → X + H2O
nH2 = nH2O => mH2O = 0,18.18 = 3,24 gam
Áp dụng ĐLBT khối lượng => mX = mH2 + mCuO + mFe3O4 - mH2O = 16,72 gam.