Cho a gam nhôm cacbua tác dụng với lượng nước (dư) thu được khí A. Đốt cháy hoàn toàn A trên cần 6,272 lít khí oxi . Giá trị của a=?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



| CHÚ Ý |
| Với ancol thì mỗi một nguyên tử C chỉ có thể đính với một nhóm –OH nên khi ta thấy số mol CO2 = số mol OH thì các ancol phải là ancol no. Vì khi đó ancol không thể có liên kết . |

\(n_{KMnO_4}=\dfrac{18.96}{158}=0.12\left(mol\right)\)
\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
\(0.12...........................................0.06\)
\(V_{O_2}=0.06\cdot22.4=1.344\left(l\right)\)
\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(4Al+3O_2\underrightarrow{t^0}2Al_2O_3\)
\(0.08.....0.06.......0.04\)
\(m_{Al\left(dư\right)}=\left(0.2-0.08\right)\cdot27=3.24\left(g\right)\)
\(m_{Al_2O_3}=0.04\cdot102=4.08\left(g\right)\)

a, \(2Mg+O_2\underrightarrow{^{t^o}}2MgO\)
\(n_{MgO}=\dfrac{2}{40}=0,05\left(mol\right)\)
\(n_{O_2}=\dfrac{1}{2}n_{MgO}=0,025\left(mol\right)\Rightarrow V_{O_2}=0,025.22,4=0,56\left(l\right)\)
b, Có lẽ đề cho oxi tác dụng với hidro chứ không phải oxit bạn nhỉ?
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PT: \(2H_2+O_2\underrightarrow{^{t^o}}2H_2O\)
Xét tỉ lệ: \(\dfrac{0,15}{2}>\dfrac{0,025}{1}\), ta được H2 dư.
THeo PT: \(n_{H_2O}=2n_{O_2}=0,05\left(mol\right)\Rightarrow m_{H_2O}=0,05.18=0,9\left(g\right)\)

Em đăng tách câu hỏi ra nhé!
---
Bài 1:
Na2CO3 + CaCl2 -> 2 NaCl + CaCO3
m(kt)=mCaCO3=20(g)
-> nCaCO3=0,2(mol)
-> nNa2CO3=0,2(mol)
=> m= mNa2CO3=0,2.106=21,2(g)
Bài 2:
nC=3,6/12=0,3(mol)
C+ O2 -to-> CO2
nCO2=nC=0,3(mol)
=>V=V(CO2,đktc)=0,3.22,4=6,72(l)


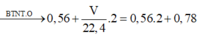

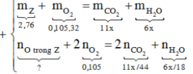
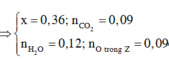
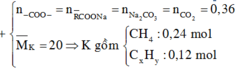

Đặt \(n_{Al_4C_3}=x\left(mol\right);n_{O_2}=\dfrac{6,272}{22,4}=0,28\left(mol\right)\)
PTHH: \(Al_4C_3+12H_2O\rightarrow4Al\left(OH\right)_3\downarrow+3CH_4\uparrow\)
x--------------------------------------->3x
\(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
3x---->6x
=> 6x = 0,28 => \(x=\dfrac{7}{150}\left(mol\right)\)
=> \(a=m_{Al_4C_3}=\dfrac{7}{150}.144=6,72\left(g\right)\)