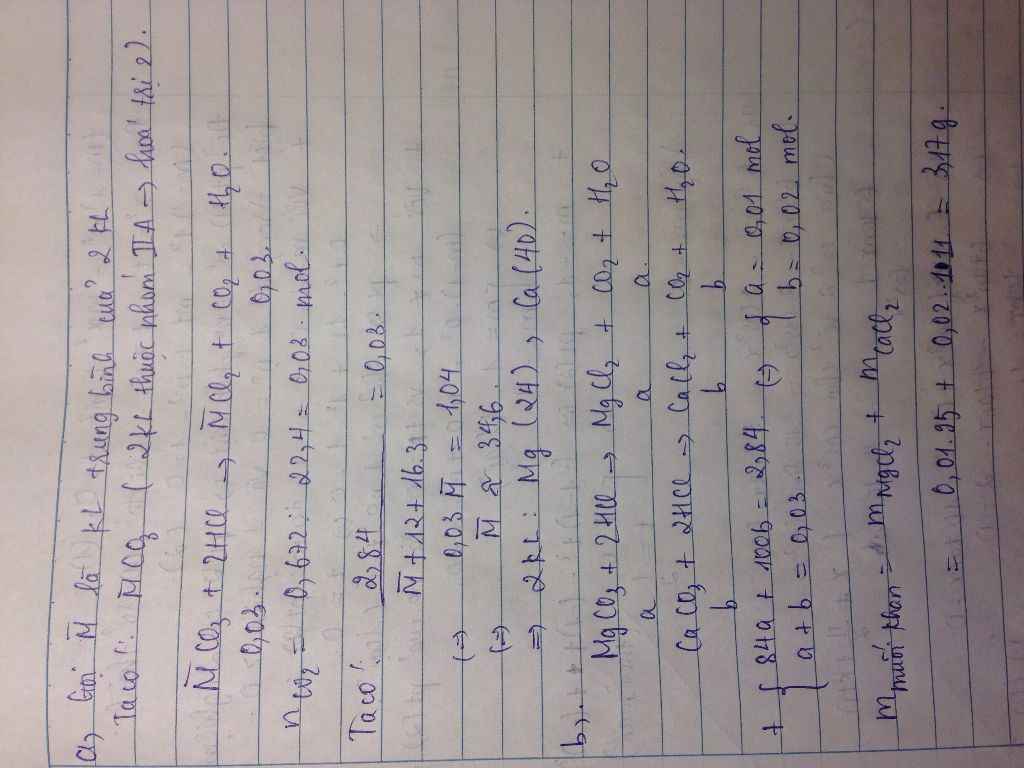Hòa tan hoàn toàn 12,6 g một muối muối cacbonat của kim loại hóa trị II vào dung dịch H2SO4 loãng thu được 3,36 lít khí ở điều kiện tiêu chuẩn. Tìm CTHH của muối cacbonat
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Đặt công thức của hai muối là RCO3
Ta có: nCO2= 10,08/22,4= 0,45 mol
RCO3+ 2HCl → RCl2+ CO2+ H2O
Theo PT ta có: nRCO3= nRCl2= nCO2= 0,45 mol
→mRCl2- mRCO3= 0,45. (R+71)- 0,45. (R+60)= 4,95 gam
→Muối sau phản ứng tăng so với trước phản ứng là 4,95 gam

Đáp án C
Gọi công thức của hai muối trong hỗn hợp ban đầu là A2CO3 và BCO3.
Có các phản ứng:
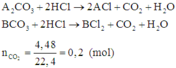
Quan sát phản ứng thấy khi cho hỗn hợp phản ứng với dung dịch HCl thì mỗi gốc C O 3 2 - trong muối được thay thế bởi hai gốc Cl-.
Có 1 mol C O 3 2 - bị thay thế bởi 2 mol Cl- thì khối lượng của muối tăng: (2.35,5 -60) = 11(gam)
Do đó khối lượng muối khan thu được khi cô cạn dung dịch là:
mmuối clorua = mmuối cacbonat + 0,2.11 = 23,8 + 0,2.11= 26 (gam)

Câu 5:
\(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
PTHH: ACO3 + 2HCl --> ACl2 + CO2 + H2O
_____0,04<-----------------------0,04
=> \(M_{ACO_3}=\dfrac{4}{0,04}=100\left(g/mol\right)\)
=> MA 40 (g/mol)
=> A là Ca => CTHH của muối là CaCO3
Câu 6:
\(n_{Na_2O}=\dfrac{3,1}{62}=0,05\left(mol\right)\)
PTHH: Na2O + H2O --> 2NaOH
______0,05--------------->0,1
=> \(C_M=\dfrac{0,1}{0,2}=0,5M\)

Chọn đáp án C
• muối cacbonat kim loại hóa trị II: MCO3 + 2HCl → MCl2 +CO2↑ + H2O
• muối cacbonat kim loại hóa trị I: N2CO3 + 2HCl → 2NCl + CO2↑ + H2O
từ tỉ lệ phản ứng có: ∑nHCl = 2∑nCO2↑ = 0,09 mol.
m gam muối khi cô cạn A là muối clorua, là sự thay thế 1 gốc CO32− bằng 2 gốc Cl.
⇒ tăng giảm khối lượng có: m = mmuối clorua = 21 + (0,09 × 35,5 – 0,045 × 60) = 21,495 gam.
⇒ Chọn đáp án C.