Cho 200ml dd H3PO4 1.5M td với 200ml dd NAOH 2M. Sau khi phản ứng xảy ra hoàn toàn, đem cô cạn dd. Khối lượng muối khan thu được là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

$n_{CH_3COOC_2H_5} = \dfrac{8,8}{88} = 0,1(mol)$
$n_{NaOH} = 0,2.2 = 0,4(mol) > n_{este}$ nên NaOH dư
$CH_3COOC_2H_5 + NaOH \to CH_3COONa + C_2H_5OH$
$n_{C_2H_5OH} = n_{este} = 0,1(mol)$
Bảo toàn khối lượng :
$m_{chất\ rắn} = 8,8 + 0,4.40 - 0,1.46 = 20,2(gam)$

Theo gt ta có: $n_{C_3H_5COOCH_3}=0,086(mol);n_{NaOH}=0,04(mol)$
$\Rightarrow n_{CH_3OH}=0,04(mol)$
Bảo toàn khối lượng ta có: $m_{chatran}=8,92(g)$

Đáp án B
Hướng dẫn giải:
Ta có: nH3PO4= 0,3 mol; nNaOH= 0,5 mol
Ta có 1< T= nNaOH/ nH3PO4=1,67<2
→ NaOH tác dụng với H3PO4 theo 2PTHH:
NaOH + H3PO4 → NaH2PO4+ H2O
2NaOH + H3PO4 → Na2HPO4+ 2H2O
Đặt nNaH2PO4= x mol; nNa2HPO4= y mol
Ta có nH3PO4= x+ y= 0,3 mol; nNaOH= x + 2y= 0,5 mol → x=0,1; y= 0,2
→ mNaH2PO4= 12gam; mNa2HPO4=28,4 gam

\(n_{Mg}=0,3\left(mol\right)\)
\(n_{HCl}=0,3\left(mol\right)\)
\(PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\)
...............0,15......0,3..........0,15.....0,15......
- Thấy sau phản ứng HCl phản ứng hết, Mg còn dư ( dư 0,15 mol )
\(\Rightarrow\left\{{}\begin{matrix}m_M=m_{MgCl_2}=14,25\left(g\right)\\V=V_{H_2}=3,36\left(l\right)\end{matrix}\right.\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
\(n_{HCl}=0,2.1,5=0,3\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,3}{2}\), ta được Mg dư.
Theo PT: \(n_{MgCl_2}=n_{H_2}=\dfrac{1}{2}n_{HCl}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{MgCl_2}=0,15.95=14,25\left(g\right)\\V_{H_2}=0,15.22,4=3,36\left(l\right)\end{matrix}\right.\)
Bạn tham khảo nhé!

Đáp án A
nOH- = 0,375 mol, nH3PO4 = 0,2 mol
Có T = nOH-/ nH3PO4 = 0,375/0,2 = 1,875
Nên sau phản ứng thu được 2 loại muối là H2PO4- và HPO42-
H3PO4+ OH- → H2PO4-+ H2O
x mol x x mol
H3PO4+ 2OH-→ HPO42-+ 2H2O
y mol 2y y mol
Ta có x+y = 0,2; x+2y = 0,375 nên x = 0,025 mol; y = 0,175 mol
Dung dịch X có Na+: 0,125 mol; Ba2+: 0,125mol; H2PO4-: 0,025mol; HPO42-: 0,175 mol
Khối lượng muối khi cô cạn là
0,125.23+ 0,125.137+ 0,025.97+ 0,175.96 = 39,225 gam

Chọn D
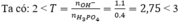
Vậy sau phản ứng thu được hai muối Na 2 HPO 4 (x mol) và Na 3 PO 4 (y mol)
Bảo toàn Na có: 2x + 3y = 1,1 (1)
Bảo toàn C có: x + y = 0,4 (2)
Từ (1) và (2) có x = 0,1 và y = 0,3 mol
Vậy khối lượng Na 2 HPO 4 và Na 3 PO 4 lần lượt là 14,2 gam và 49,2 gam.

n(AgNO3) = 1.0,2 = 0,2mol
2AgNO3 + M → M(NO3)2 + 2Ag
0,2 0,1 m
[M(NO3)2] = 0,1(M+124) = 18,8g
→ M = 64. M là Cu
=> Đáp án D
$n_{H_3PO_4} = 0,2.1,5 = 0,3(mol)$
$n_{NaOH} = 0,2.2 = 0,4(mol)$
Ta thấy : $1 < n_{NaOH} : n_{H_3PO_4} < 2$ nên sản phẩm gồm $NaH_2PO_4(a\ mol) ; Na_2HPO_4(b\ mol)$
$H_3PO_4 + NaOH \to NaH_2PO_4 + H_2O$
$H_3PO_4 + 2NaOH \to Na_2HPO_4 + 2H_2O$
Theo PTHH :
$n_{NaOH} = a + 2b = 0,4 ; n_{H_3PO_4} = a + b = 0,3$
Suy ra : a = 0,1 ; b = 0,1
$\Rightarrow m_{muối} = 0,1.120 + 0,1.142 = 26,2(gam)$