Bài 24*: Khử hoàn toàn m gam một oxit sắt cần dùng 5,376 lít khí H2 (đktc), thu lấy kim loại sắt sinh ra cho tác dụng với dung dịch HCl dư thì thấy thoát ra 4,032 lít H2 (đktc). Tìm công thức hóa học của oxit sắt và tính giá trị m. Biết phản ứng của Fe với dung dịch HCl tạo ra muối sắt (II).
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


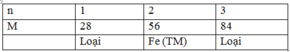
Ta có bảng sau:
n |
1 |
2 |
3 |
4 |
M |
21 (loại) |
42 (loại) |
63 (loại) |
84 (loại) |
=> loại trường hợp này


Đáp án : B
m H 2 S O 4 = 98g => mdd sau = 103,6g
=> n H 2 O t h ê m = 0,2 mol => nO(oxit) = 0,2 mol
Khi cho Fe + HCl : n H 2 = 0,15 mol = nFe
=> nFe : nO = 0,15 : 0,2 = 3 : 4
=> Fe3O4

CuO + H2 => Cu +H2O
a => a => a
FexOy +yH2 => xFe + yH2O
a => ay => ax
Fe + 2Hcl => FeCl2 + h2
0,02 <= 0,02
Ta có n O p/ư= (2,4-1,76): 16=0,04= ay +y => a = 0,04/(y+1)
Mặt khác : ax= 0,02 => a =0,02/x
=> x = 2 , y =3
Fe2O3
Khối lượng chất rắn giảm chính là khối lượng oxi.
-->nO= (2,4 - 1,76)/16 = 0,04 mol -->mO=0,64(g)
Ta có nFe=nH2=0,02.-->mFe=1,12(g)
Ta có m(hỗn hợp BĐ)= mCu+mFe+mO=2,4
-->mcu= 0,64 -->nCu=0,01mol
Hỗn hợp ban đầu có: CuO: 0,01 mol
FexOy: a mol
Ta có nO=0,01+ya=0,04-->ya=0,03
nFe=xa=0,02
Ta có nFe/nO=2/3
Vậy oxit sắt là Fe2O3.

PTHH: AxOy + yCO --to--> xA + yCO2
Có: nCO(dư) + nCO2 = nCO(bd) = \(\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Mà \(\dfrac{28.n_{CO\left(dư\right)}+44.n_{CO_2}}{n_{CO}+n_{CO_2}}=20,4.2=40,8\)
=> nCO2 = 0,048 (mol)
\(n_{A_xO_y}=\dfrac{2,784}{x.M_A+16y}\left(mol\right)\)
AxOy + yCO --to--> xA + yCO2
=> \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2,784y}{x.M_A+16y}=0,048\left(mol\right)\left(1\right)\\n_A=\dfrac{2,784x}{x.M_A+16y}\left(mol\right)\end{matrix}\right.\)
(1) => \(M_A=\dfrac{42y}{x}=>\dfrac{y}{x}=\dfrac{M_A}{42}\) (2)
PTHH: 2A + 2nHCl --> 2ACln + nH2
=> \(n_{H_2}=\dfrac{1,392xn}{x.M_A+16y}=0,036\left(mol\right)\)
=> \(1,392n=0,036.M_A+\dfrac{0,576y}{x}\) (3)
(2)(3) => MA = 28n
Xét n = 1 => L
Xét n = 2 => MA = 56 (Fe) => \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
Xin cảm ơn mọi người đã đọc câu hỏi này nhưng em đã nghĩ ra đáp án cho bài tập này rồi ạ

CTHH: AxOy
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
PTHH: AxOy + yH2 --to--> xA + yH2O
\(\dfrac{0,06}{y}\)<--0,06---->\(\dfrac{0,06x}{y}\)
2A + 2nHCl --> 2ACln + nH2
\(\dfrac{0,06x}{y}\)---------------->\(\dfrac{0,03xn}{y}\)
=> \(\dfrac{0,03xn}{y}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\)
=> \(\dfrac{y}{x}=\dfrac{2}{3}n\)
\(M_{A_xO_y}=\dfrac{3,48}{\dfrac{0,06}{y}}=58y\left(g/mol\right)\)
=> \(x.M_A=42y\)
=> \(M_A=\dfrac{42y}{x}=28n\left(g/mol\right)\)
Xét n = 2 thỏa mãn => MA = 56 (g/mol)
=> A là Fe
\(\dfrac{x}{y}=\dfrac{3}{2n}=\dfrac{3}{4}\) => CTHH: Fe3O4



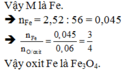
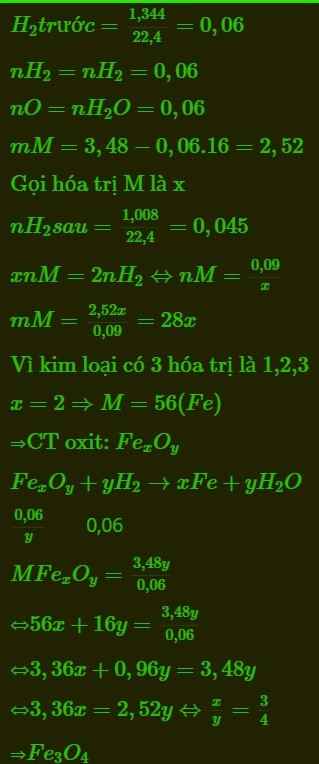
\(CT:Fe_xO_y\)
\(Fe_xO_y+yH_2\underrightarrow{^{t^o}}xFe+yH_2O\left(1\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\)
\(n_{Fe}=n_{H_2\left(2\right)}=\dfrac{4.032}{22.4}=0.18\left(mol\right)\)
\(n_{H_2\left(1\right)}=\dfrac{y}{x}\cdot n_{Fe}=\dfrac{5.376}{22.4}=0.24\left(mol\right)\)
\(\Leftrightarrow\dfrac{y}{x}\cdot0.18=0.24\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
\(CT:Fe_3O_4\)
\(m_{Fe_3O_4}=\dfrac{0.18}{3}\cdot232=13.92\left(g\right)\)