một loại khí thiên nhiên có tahnhf phần phần trăm về thể tích các khí như sau 85%(CH4), 10% (C2H6), 2% (nito)và 3 % (CO2) . tính số mol ko khí dùng để đốt cháy hết 1 mol khí trên bt khí Oxi chiếm 20 thể tích ko khí và các khí đo cùng ở điều kiện về nhiệt độ và áp suất
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1. Trong 1000 m 3 khí thiên nhiên có 850 m 3 C H 4
2 C H 4 → 1500 ° C C 2 H 2 + 3 H 2
CH ≡ CH + HCl → 150 - 200 ° C , H g C l 2 C H 2 = C H - C l
Khối lượng vinyl clorua thu được (nếu hiệu suất các quá trình là 100%) là:
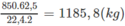
Với hiệu suất cho ở đầu bài, khối lượng vinyl clorua là:
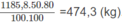
2. Nhiệt lượng cần dùng để làm nóng 100 lít nước từ 20 ° C lên 100 ° C :
100.4,18.(100 - 20) = 33440 (kJ)
Vì 20% nhiệt lượng đã toả ra môi trường nên nhiệt lượng mà khí thiên nhiên cần cung cấp phải là :
Đặt số mol C 2 H 6 tà x thì số mol C H 4 là 85. 10 - 1 x.
Ta có 1560x + 88085. 10 - 1 x = 41800
x = 462. 10 - 2
Thể tích khí thiên nhiên cần dùng:
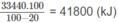

n CH4 = 1.85% = 0,85(mol)
n C2H6 = 1.10% = 0,1(mol)
$CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
$C_2H_6 + \dfrac{7}{2} O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O$
Theo PTHH :
n O2 = 2n CH4 + 7/2 n C2H6 = 2,05(mol)
n không khí = n O2 : 20% = 2,05 : 20% = 10,25(mol)

1. Trong 1000 m 3 khí thiên nhiên có 850 m 3 C H 4
2 C H 4 → 1500 ° C C 2 H 2 + 3 H 2
CH ≡ CH + HCl → 150 - 200 ° C , H g C l 2 C H 2 = C H - C l
Khối lượng vinyl clorua thu được (nếu hiệu suất các quá trình là 100%) là:
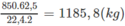
Với hiệu suất cho ở đầu bài, khối lượng vinyl clorua là:
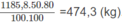
2. Nhiệt lượng cần dùng để làm nóng 100 lít nước từ 20 ° C lên 100 ° C :
100.4,18.(100 - 20) = 33440 (kJ)
Vì 20% nhiệt lượng đã toả ra môi trường nên nhiệt lượng mà khí thiên nhiên cần cung cấp phải là :
Đặt số mol C 2 H 6 tà x thì số mol C H 4 là 85. 10 - 1 x.
Ta có 1560x + 88085. 10 - 1 x = 41800
x = 462. 10 - 2
Thể tích khí thiên nhiên cần dùng:
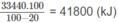

a)
CH4 + 2O2 --to--> CO2 + 2H2O
2C2H6 + 7O2 --to--> 4CO2 + 6H2O
b) \(n_{CH_4}=\dfrac{85\%.112}{22,4}=4,25\left(mol\right)\)
\(n_{C_2H_6}=\dfrac{112.10\%}{22,4}=0,5\left(mol\right)\)
=> \(Q=4,25.880+0,5.1560=4520\left(kJ\right)\)
c) \(Q=2000.4,18.\left(100-20\right)=668800\left(J\right)=668,8\left(kJ\right)\)
Giả sử có a mol khí thiên nhiên
=> \(\left\{{}\begin{matrix}n_{CH_4}=a.85\%=0,85a\left(mol\right)\\n_{C_2H_6}=a.10\%=0,1a\left(mol\right)\end{matrix}\right.\)
\(Q=880.0,85a+1560.0,1a=668,8\left(kJ\right)\)
=> a = \(\dfrac{418}{565}\left(mol\right)\) => \(V=\dfrac{418}{565}.22,4=16,572\left(l\right)\)

a, Ta có: \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\Rightarrow n_H=0,6.2=1,2\left(mol\right)\)
m = mC + mH = 0,4.12 + 1,2.1 = 6 (g)
b, Theo ĐLBT KL, có: m + mO2 = mCO2 + mH2O
⇒ mO2 = 22,4 (g) \(\Rightarrow n_{O_2}=\dfrac{22,4}{32}=0,7\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,7.22,4=15,68\left(g\right)\)
\(\Rightarrow V_{kk}=\dfrac{15,68}{20\%}=78,4\left(g\right)\)